불과 몇 년 전만 해도 “한 번 죽은 뇌세포는 재생되지 않는다”는 말이 상식처럼 통용되었지만, 2026년 2월에 발표된 최신 연구들은 이 오래된 도그마를 완전히 무너뜨리고 있습니다.
이제 뇌과학은 단순히 질병을 치료하는 단계를 넘어, 우리가 어떻게 하면 80세, 100세가 되어서도 20대의 명석함을 유지할 수 있는지, 그리고 우리의 감정과 기억이 뇌의 어떤 미세한 움직임 속에서 탄생하는지를 실시간으로 추적하고 있습니다.
이번에는 Cell, Nature, Science, The Lancet, NEJM 등 세계 최고의 저널들이 2026년 2월 한 달간 쏟아낸 경이로운 발견들을 모아보았습니다.
인지적 탄력성과 신경 발생의 비밀
나이가 들어도 인지 기능이 쇠퇴하지 않는 이른바 ‘슈퍼 에이저(SuperAgers)’의 비밀이 마침내 풀리고 있습니다.
과거에는 단순히 유전적인 운이라고 생각했던 영역들이 사실은 뇌의 적극적인 신경 발생과 후성유전학적 조절의 결과임이 밝혀졌습니다.
건강한 고령자의 뇌세포는 멈추지 않고 태어난다
성인의 뇌에서도 새로운 뉴런이 만들어진다는 ‘성인 신경 발생(Adult Neurogenesis)’ 이론은 수십 년간 뇌과학계의 뜨거운 감자였습니다.
하지만 2026년 2월 25일, Nature에 발표된 오를리 라자로프(Orly Lazarov) 교수팀의 연구는 이 논쟁에 강력한 종지부를 찍었습니다.[1]
연구진은 사후 인간 뇌 조직을 정밀 분석한 결과, 80세 이상의 고령자 중 20~30대 수준의 기억력을 유지하는 ‘슈퍼 에이저’들의 해마에서 일반 노인보다 약 2배 더 많은 미성숙 뉴런이 발견된다는 사실을 입증했습니다.[1, 2, 3]
이 연구는 단순히 뉴런의 숫자를 세는 것에 그치지 않고, 알츠하이머병(AD) 환자와 슈퍼 에이저의 뇌를 직접적으로 비교했다는 점에서 혁신적입니다.
연구 결과, 알츠하이머 환자의 뇌에서도 신경 줄기세포(NSCs) 자체는 존재하고 있었습니다.
그러나 이 줄기세포들이 성숙한 뉴런으로 분화하는 과정이 차단되어 있었던 반면, 슈퍼 에이저들은 이 과정이 매우 활발하게 일어나고 있었습니다.[1]
이는 인지 저하가 노화의 피할 수 없는 운명이 아니라, 뇌 내의 ‘신경 분화 스위치’를 어떻게 켜느냐의 문제임을 시사합니다.[2]
| 뇌 상태 분류 | 신경 줄기세포(NSCs) 상태 | 미성숙 뉴런 활성도 | 인지적 특징 |
|---|---|---|---|
| 건강한 청년 (YA) | 매우 풍부함 | 매우 높음 | 기준 인지 능력 |
| 건강한 노인 (HA) | 감소함 | 낮음 | 완만한 인지 저하 |
| 알츠하이머 환자 (AD) | 풍부하나 분화 정체 | 극도로 낮음 | 심각한 기억력 상실 |
| 슈퍼 에이저 (SA) | 적정 수준 유지 | 일반 노인의 2배 | 청년 수준의 기억력 |
이 데이터는 성인 해마 신경 발생이 실제로 인간의 고등 인지 기능에 기여한다는 사실을 강력하게 지지합니다.[1]
펜실베이니아 대학교의 송홍준(Hongjun Song) 박사는 “알츠하이머 환자의 뇌에 여전히 신경 줄기세포가 존재한다는 사실은, 이들을 다시 활성화하여 미성숙 뉴런으로 분화시키는 것이 새로운 치료 전략이 될 수 있음을 보여준다”고 평가했습니다.[1]
Zinc-Finger와 Open Chromatin
슈퍼 에이저와 알츠하이머 환자의 뇌를 결정적으로 가르는 것은 유전자 그 자체가 아니라 유전자의 ‘포장 상태’, 즉 염색질의 상태였습니다.
이번 연구에서는 메신저 RNA(mRNA) 수준의 차이보다 ‘열린 염색질(Open Chromatin)’ 영역의 패턴에서 더 뚜렷한 차이가 나타났습니다.[1]
후성유전학이란 유전자의 염기서열은 변하지 않으면서 세포가 유전자를 읽는 방식을 조절하는 학문입니다.
뇌세포 내에서 특정 유전자가 발현되기 위해서는 꽁꽁 묶여 있던 유전 단백질인 염색질이 느슨하게 풀려야 하는데, 이를 ‘열린 염색질’이라고 합니다.
슈퍼 에이저의 뇌세포는 신경 발생과 관련된 핵심 유전자 부위가 활짝 열려 있어 뉴런 재생이 원활한 반면, 알츠하이머 환자의 뇌는 이 부위가 닫혀 있었습니다.[1]
특히 아연 집게(Zinc-finger, ZNF) 계열의 전사 인자들이 이 과정을 조절하는 핵심 스위치라는 사실이 밝혀지면서, 향후 후성유전학적 치료제의 표적이 될 가능성을 열어주었습니다.[1]
대상포진 백신이 치매 예방의 새로운 구원투수?
전혀 예상치 못한 곳에서 치매 예방의 실마리가 발견되었습니다.
2026년 2월, The Lancet Neurology에 발표된 파스칼 겔드세처(Pascal Geldsetzer) 박사의 연구는 전 세계 뇌과학계를 깜짝 놀라게 했습니다.[4]
연구팀은 캐나다 온타리오주의 독특한 백신 정책을 활용한 ‘자연 실험’ 결과를 공개했는데,
1946년 1월 1일 이후 출생하여 대상포진 백신(Zostavax)을 무료로 접종받을 자격을 얻은 그룹이 그렇지 못한 그룹에 비해 치매 진단율이 무려 2% 낮게 나타났습니다.[4]
이 연구는 특정 바이러스나 병원균이 뇌 내 만성 염증을 유발하여 치매 발병을 가속화할 수 있다는 ‘감염 가설’에 힘을 실어줍니다.
대상포진 바이러스의 재활성화를 백신으로 막는 것이 단순히 피부 발진을 예방하는 것을 넘어, 뇌의 신경 면역 체계를 보호하는 부수적인 효과를 냈을 가능성이 크기 때문입니다.[4]
겔드세처 박사는 “Zostavax와 같은 약독화 생백신은 면역 체계 전반에 광범위한 ‘부스팅’ 효과를 주어, 노화로 인한 인지 기능 저하를 늦출 수 있다”고 설명했습니다.[4]
별아교세포와 뇌의 정보 처리 시스템
오랫동안 뇌의 주인공은 전기를 내뿜는 뉴런(Neuron)이었습니다.
하지만 2026년 2월, 그동안 ‘조연’이나 ‘영양 공급원’으로만 여겨졌던 별아교세포(Astrocyte)가 뇌의 고등 기능을 지휘하는 ‘숨은 지휘자’임이 밝혀졌습니다.
공포 기억을 실시간으로 조절하는 별아교세포
우리가 과거의 무서운 경험을 기억하고, 시간이 지나 그 공포에서 벗어나는 과정에 별아교세포가 결정적인 역할을 한다는 사실이 Nature에 게재되었습니다.[5]
애리조나 대학교의 린지 할러데이(Lindsay Halladay) 교수팀은 쥐 실험을 통해 별아교세포가 단순히 뉴런을 보조하는 수준을 넘어, 감정 상태를 동적으로 추적하고 공포 반응을 조직한다는 사실을 발견했습니다.[5]
별아교세포는 뉴런처럼 전기 신호를 사용하지 않고 칼슘 이온(Ca2+)의 흐름을 통해 소통합니다.
연구팀이 쥐의 별아교세포 칼슘 신호를 차단하자, 쥐들은 학습된 공포를 제대로 회상하지 못했을 뿐만 아니라, 위험 상황이 끝난 뒤에도 공포를 잊는 ‘소거(Extinction)’ 과정에 큰 어려움을 겪었습니다.[5]
이는 별아교세포가 부적절한 공포 반응을 억제하고 정서적 적응을 돕는 ‘감정의 컨트롤러’임을 의미합니다.
기저외측 편도체(Basolateral Amygdala, BLA)의 역할
편도체는 뇌에서 공포와 위협을 감지하는 핵심 센터입니다. 이번 연구는 특히 ‘기저외측 편도체’ 내의 별아교세포 활동에 주목했습니다.[5]
- 학습 단계: 쥐가 특정 소리와 전기 충격을 연결할 때 별아교세포의 칼슘 활동이 급증합니다.
- 회상 단계: 소리만 들려주어도 별아교세포는 이전의 학습 패턴을 재현하며 공포 반응(얼어붙음)을 유도합니다.
- 소거 단계: 충격 없이 소리만 반복될 때 별아교세포는 새로운 활동 패턴을 형성하여 공포를 ‘톤 다운’ 시킵니다.[5]
이러한 발견은 외상 후 스트레스 장애(PTSD)나 불안 장애 환자들이 왜 특정 기억에서 벗어나지 못하는지를 설명할 수 있는 새로운 경로를 제시합니다.
미래의 치료법은 뉴런의 전기적 신호를 조절하는 대신, 별아교세포의 칼슘 신호를 미세 조정하는 방식이 될 수도 있습니다.[5]
뇌의 새로운 수문장: ‘기저 장벽 세포(Base Barrier Cells)’
뇌를 외부 유해 물질로부터 보호하는 혈액-뇌 장벽(BBB) 외에, 또 다른 강력한 방어선이 발견되었습니다.
Nature Neuroscience 2월호에 발표된 비브-유겐트(VIB-UGent) 연구팀의 논문에 따르면, 뇌실맥락얼개(Choroid Plexus) 기저부에 위치한 독특한 세포 집단이 뇌척수액과 혈류 사이의 물질 교환을 엄격히 통제하는 ‘제2의 장벽’ 역할을 한다는 것이 확인되었습니다.[6]
연구팀은 이 세포들을 ‘기저 장벽 세포 (Base Barrier Cells)’라고 명명했습니다. 이들은 강력한 밀착 연접(Tight Junction)이라는 분자 리벳으로 서로 꽉 조여져 있어, 평상시에는 혈액 속의 미세한 분자조차 뇌로 함부로 들어오지 못하게 막습니다.[6]
하지만 전신 염증(패혈증 등)이 발생하면 이 장벽 세포들이 취약해지며 뇌 내부로 유해 물질이 침투하는 통로가 됩니다.
이 세포들은 인간의 뇌에서도 동일하게 존재하며, 뇌수막염이나 신경 염증성 질환 치료의 새로운 타깃이 될 전망입니다.[6]
새로운 임상적 돌파구
2026년 2월은 소아기 질환부터 치명적인 암에 이르기까지, 뇌와 관련된 다양한 임상 시험에서 괄목할 만한 성과가 보고된 달이기도 합니다.
소아 편두통 예방: 프리마네주맙(Fremanezumab)
어린아이들이 겪는 편두통은 학업과 사회적 성장에 치명적인 영향을 미치지만, 그동안 성인에 비해 치료 옵션이 매우 제한적이었습니다.
The New England Journal of Medicine(NEJM)은 2월 27일, 6세에서 17세 사이의 소아 및 청소년 환자들을 대상으로 한 프리마네주맙의 임상 3상 결과를 전격 발표했습니다.[7, 8]
칼슘 유전자 관련 펩타이드(CGRP)를 표적으로 하는 이 항체 치료제는 임상 결과 위약 대비 압도적인 효과를 보여주었습니다.
| 평가 항목 | 위약(Placebo) 그룹 | 프리마네주맙 투여군 | 통계적 유의성(P-value) |
|---|---|---|---|
| 월평균 편두통 일수 감소 | 1.4일 감소 | 2.5일 감소 | P = 0.02 |
| 심각한 두통 발생 일수 감소 | 1.5일 감소 | 2.6일 감소 | P = 0.02 |
| 편두통 50% 이상 감소 비율 | 27.0% | 47.2% | P = 0.002 |
이 연구는 소아 편두통 환자들에게 안전하고 효과적인 예방 치료의 길을 열어주었으며, 주된 부작용은 주사 부위의 경미한 발적(Erythema)에 그쳤습니다.[7]
이는 CGRP 경로 억제가 어린이들의 뇌에서도 성인과 유사한 안전성과 유효성을 가짐을 입증한 것입니다.
[이해를 위한 개념] CGRP란 무엇인가?
CGRP(Calcitonin Gene-Related Peptide)는 통증 신호를 전달하고 뇌혈관을 확장시키는 신경전달물질입니다.
편두통이 시작될 때 뇌에서는 CGRP 수치가 급격히 상승하며, 이것이 혈관 주변의 신경을 자극해 극심한 통증을 유발합니다.[7]
프리마네주맙은 이 CGRP 분자에 직접 결합하여 수용체와 만나지 못하게 방해함으로써, 통증의 시작점 자체를 차단하는 역할을 합니다.[7]
당뇨병 약 메트포르민, 가장 공격적인 뇌암 ‘교모세포종’을 사냥
교모세포종(Glioblastoma)은 수술이 어렵고 재발이 잦아 뇌암 중에서도 가장 치명적인 것으로 악명이 높습니다.
그런데 2026년 2월, 저널 Cells에는 당뇨병 치료제로 널리 쓰이는 메트포르민(Metformin)이 교모세포종 세포의 사멸을 유도한다는 흥미로운 연구가 실렸습니다.[9]
연구팀에 따르면, 메트포르민은 AMPK/FoxO3a 신호 경로를 활성화하여 암세포의 생존과 약물 저항성에 필수적인 ‘서바이빈(Survivin)’이라는 단백질을 억제합니다.[9]
실제 쥐 실험에서도 메트포르민을 투여한 경우 종양 조직에서 서바이빈 수치가 급감하고 암세포의 증식이 억제되는 것이 관찰되었습니다.[9]
이미 전 세계적으로 안전성이 검증된 저렴한 당뇨병 약이 치명적인 뇌암 치료의 보조제로 재탄생할 수 있는 가능성을 보여준 것입니다.[9]
Glioblastoma 란?
‘Glioblastoma‘라는 이름은 세 가지 그리스어 어근이 합쳐진 단어입니다.
- Glio- (glia): 그리스어로 ‘아교(Glue/풀)‘를 의미합니다. 뇌에서 신경세포 사이를 메우고 지지하는 ‘신경아교세포(Glial cell)’에서 유래한 종양임을 뜻합니다.
- -blast (blastos): 그리스어로 ‘싹(Sprout)’ 또는 ‘아세포(미성숙 세포)‘를 의미합니다. 세포가 성숙하지 못하고 원시적인 상태에서 매우 빠르게 분열하는 특성을 나타냅니다.
- -oma: 의학 용어에서 ‘종양(Tumor)‘을 뜻하는 접미사입니다.
[종합적 의미]: 신경아교세포 중에서도 매우 미성숙하고 분화가 덜 된 세포들이 폭발적으로 증식하여 만들어진 종양이라는 뜻입니다.
아프리카 수면병 치료의 혁명: 아코지보롤(Acoziborole)
Lancet Neurology와 Sanofi의 발표에 따르면, 기생충이 중추신경계를 침범하여 발생하는 ‘아프리카 수면병’에 대한 획기적인 치료제가 개발되었습니다.[10]
아코지보롤(Acoziborole)이라 불리는 이 약물은 단 세 알의 알약을 한 번만 복용하면 치료가 끝나는 ‘싱글 도즈(Single-dose)’ 치료제입니다.
과거에는 수면병 치료를 위해 비소 유도체와 같이 독성이 강하고 복잡한 입원 치료가 필요했습니다.
하지만 아코지보롤은 뇌-혈관 장벽을 효과적으로 통과하여 중추신경계 내의 기생충을 박멸할 수 있으며, 입원 없이 집에서 복용이 가능합니다.[10]
이는 의료 인프라가 부족한 아프리카 소외 지역에서 수면병을 완전히 퇴치할 수 있는 게임 체인저가 될 것으로 보입니다.
아프리카 수면병이란?
아프리카 수면병(African sleeping sickness)은 공식 명칭으로 ‘인간 아프리카 파동편모충증(human African trypanosomiasis)’이라고 불리며, 주로 중앙 및 서아프리카 지역에서 감염된 체체파리(tsetse fly)에 물려 전파되는 치명적인 기생충 질환입니다.
주요 특징과 증상은 다음과 같습니다:
후기 단계: 기생충이 혈액-뇌 장벽(Blood-brain barrier)을 통과해 중추신경계로 침투합니다. 이로 인해 극심한 수면 장애, 발작, 공격성, 인지 및 행동 이상, 혼란, 무기력증 등의 신경학적 증상이 발생하며, 치료받지 않으면 거의 항상 사망에 이릅니다.
초기 단계: 두통이나 발열 같은 증상이 나타납니다.
발달 장애와 조현병의 유전적 설계도
뇌가 형성되는 초기 단계에서 발생하는 사소한 오류들이 어떻게 자폐증이나 조현병과 같은 질환으로 이어지는지에 대한 정밀한 유전적 지도도 업데이트되었습니다.
자폐 스펙트럼의 새로운 범인: 산화질소와 ‘고장 난 정지 버튼’
자폐 스펙트럼 장애(ASD)의 생물학적 원인을 규명하기 위한 연구에서 산화질소(Nitric Oxide)라는 익숙한 화학 물질이 주목받고 있습니다.
2026년 2월 25일, Molecular Psychiatry에 게재된 히브리 대학교 하이탐 아말(Haitham Amal) 교수팀의 연구는 산화질소가 뇌 내에서 어떻게 ‘고장 난 버튼’처럼 작용하는지를 상세히 설명했습니다.[11]
정상적인 뇌에서 산화질소는 적절한 수준으로 신호를 조절하지만, 일부 자폐 모델에서는 산화질소가 과도하게 분비되어 ‘TSC2’라는 보호 단백질에 화학적 꼬리표(S-니트로실화)를 붙입니다.
TSC2는 원래 세포의 성장과 단백질 합성을 관리하는 ‘mTOR 경로’의 브레이크 역할을 하는데, 산화질소 때문에 TSC2가 제 기능을 못 하게 되자 mTOR 경로가 폭주(Overdrive)하게 됩니다.[11]
이로 인해 뉴런 사이의 연결이 비정상적으로 과잉 형성되거나 단백질 합성이 조절되지 않아 자폐 증상이 나타나게 되는 것입니다.
연구팀이 산화질소 합성을 억제하자 쥐의 자폐 관련 행동이 유의미하게 개선되었는데, 이는 자폐증 치료의 새로운 타깃을 정밀하게 타격할 수 있음을 의미합니다.[11]
자폐증
Autism spectrum disorder(자폐 스펙트럼 장애, ASD)는 신경발달장애(neurodevelopmental disorder)의 한 종류입니다.
자폐증은 하나의 단일한 증상이 아니라 증상의 강도와 형태가 매우 다양하게 나타나는 연속적 범위(spectrum)를 의미합니다.
자폐 스펙트럼 장애는 사회적 의사소통의 지속적 어려움과 제한적·반복적 행동 패턴을 특징으로 하며, 발달 초기부터 나타나는 신경발달장애입니다.
조현병
조현병(Schizophrenia)은 사고, 감정, 지각, 행동 등 인격의 여러 측면에서 광범위한 이상을 보이는 정신질환입니다.
과거에는 ‘정신분열병’이라 불렸으나, 거부감을 줄이고 병의 본질을 설명하기 위해 2011년 ‘조현(調絃: 거문고의 줄을 고르다)‘이라는 명칭으로 개정되었습니다.
도파민 가설: 중뇌변연계 경로(Mesolimbic pathway)에서 도파민이라는 신경전달물질이 과도하게 활성화되면 환청이나 망상 같은 ‘양성 증상’이 나타난다는 것은 임상적으로 증명된 사실입니다.
대부분의 항정신병 약물은 이 도파민 수용체를 차단하는 원리로 작동합니다.
신경 해부학적 변화: 환자의 뇌 영상(MRI) 촬영 시, 일반인에 비해 뇌실(Ventricle)이 확장되어 있거나 전두엽 및 측두엽의 부피가 소폭 감소해 있는 경우가 일관되게 관찰됩니다.
유전적 요인: 일란성 쌍둥이 중 한 명이 조현병일 경우 다른 한 명이 걸릴 확률은 약 40~50%로, 일반인(1%)에 비해 현저히 높습니다. 즉, 유전적 소인이 발병에 중요한 역할을 합니다.
TSC2와 mTOR
TSC2(Tuberous Sclerosis Complex 2)와 mTOR(mechanistic Target of Rapamycin) 경로는 세포의 성장, 증식, 그리고 대사를 조절하는 생체 내 가장 핵심적인 신호 전달 체계 중 하나입니다.
이 시스템은 영양 상태에 따라 세포를 ‘성장 모드’로 돌릴지 ‘에너지 절약 모드’로 돌릴지를 결정하는 스위치 역할을 합니다.
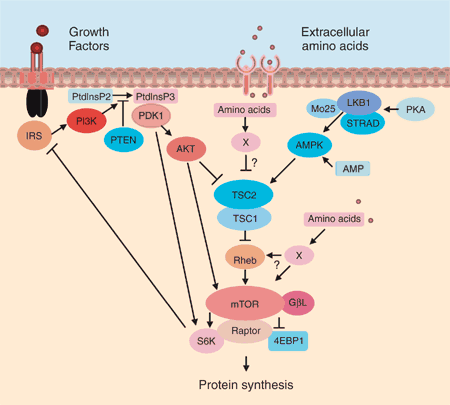
TSC 복합체의 구성: TSC2는 TSC1과 결합하여 TSC 복합체를 형성합니다. 여기서 실질적인 효소 활성(GAP 활성)을 가진 핵심 유전자는 TSC2입니다.
mTOR의 역할: mTOR는 세포 내외의 영양분(아미노산), 에너지(ATP), 성장 인자 신호를 통합하여 단백질 합성을 촉진하고 세포 성장을 주도하는 인산화 효소입니다.
음성 조절 기전 (The Brake): TSC2는 mTOR의 상위 활성제인 Rheb(레브) 단백질을 불활성화시킵니다. 즉, TSC2는 mTOR 경로를 억제하는 ‘브레이크’ 역할을 합니다.
질환과의 연관성: TSC2 유전자에 돌연변이가 생겨 브레이크가 고장 나면, mTOR가 비정상적으로 과활성화되어 온몸에 양성 종양이 생기는 결절성 경화증(Tuberous Sclerosis Complex)이 발생합니다.
조현병의 유전적 열쇠: INO80D 변이의 발견
PNAS 2026년 2월호에는 조현병 발병에 기여하는 강력한 유전적 변이가 보고되었습니다.[12]
연구진은 조현병 환자와 그 부모의 전장 유전체 시퀀싱(WGS)을 통해, 부모에게는 없지만 자녀에게만 새로 발생한 De novo Nonsense Mutation인 INO80D 유전자를 찾아냈습니다.[12]
INO80D는 염색질을 리모델링하여 유전자 발현을 조절하는 복합체의 핵심 구성 요소입니다.
이 유전자에 변이가 생기면 대뇌 피질 뉴런의 흥분성이 비정상적으로 높아지는 ‘과흥분성(Hyperexcitability)’이 나타납니다.[12]
흥미로운 점은, 이 변이가 유전자의 어느 위치에서 발생하느냐에 따라 증상의 유무가 갈린다는 것입니다.
조현병 환자에게서 발견된 변이는 유전자의 앞부분을 잘라내어 단백질 기능을 완전히 상실하게 만드는 반면, 대조군 노인에게서 발견된 변이는 끝부분에 치우쳐 있어 기능에 큰 지장이 없었습니다.[12]
이는 특정 유전자의 존재 여부보다 그 유전자의 ‘구조적 온전성’이 정신 건강에 얼마나 중요한지를 보여주는 사례입니다.
DNA 바코드: DNA 폴딩과 후성유전학적 다양성
우리 뇌에는 수천억 개의 뉴런이 있지만, 이들은 모두 동일한 유전 정보를 가지고 태어납니다.
그런데 어떻게 각기 다른 역할을 수행하는 수조 개의 연결망을 형성할 수 있을까요? 샌프란시스코 캘리포니아 대학교(UCSF)의 다니엘레 칸지오(Daniele Canzio) 박사는 그 답이 ‘DNA 폴딩(Folding)’에 있다고 말합니다.[13]
뉴런이 발달할 때, DNA는 마치 종이접기처럼 세포마다 서로 다른 방식으로 접히며 독특한 ‘바코드’를 생성합니다.
이 폴딩 패턴은 각 뉴런이 자신의 가지를 어디로 뻗어야 할지, 어떤 뉴런과 연결되어야 할지를 결정하는 정체성 역할을 합니다.[13]
지오 박사는 “만약 우리가 이 DNA 접힘의 원리를 완벽히 이해한다면, 발달 장애나 노화로 인해 망가진 뇌 회로를 다시 ‘재배선(Rewiring)’하여 기능을 회복시키는 것도 가능할 것“이라는 야심 찬 전망을 내놓았습니다.[13]
뇌공학의 미래와 AI 혁명
기술의 발전은 이제 뇌의 내부를 실시간으로 들여다보고 조작하는 수준에 이르렀습니다. 2026년 2월, 뇌공학계는 그 어느 때보다 뜨거운 한 달을 보냈습니다.
Ribo-STAMP: 뇌세포의 단백질 공장을 실시간 모니터링
유전자가 켜져 있다는 것(전사)과 실제 단백질이 만들어진다는 것(번역)은 별개의 문제입니다.
하지만 뇌의 기능을 직접적으로 수행하는 것은 단백질입니다.
스크립스 연구소(Scripps Research)와 UC 샌디에이고 연구팀은 Nature 2월 18일 자 논문에서 개별 뇌세포가 어떤 단백질을 얼마나 생산하는지 직접 측정할 수 있는 ‘Ribo-STAMP’ 기술을 공개했습니다.[14]
연구팀은 이 기술을 사용하여 쥐의 해마에 있는 20,000개의 개별 세포에서 일어나는 단백질 합성 지도를 세계 최초로 작성했습니다.
- CA1 vs CA3:
- 기억에 중요한 두 피라미드 세포는 겉보기엔 비슷하지만, CA3 뉴런의 단백질 생산 속도가 CA1보다 훨씬 높았습니다.[14]
- 이는 뇌 회로 내에서도 세포마다 ‘에너지 소비량’과 ‘업무 강도’가 다름을 시사합니다.
- 고/저 번역 상태:
- 동일한 유형의 뉴런이라도 어떤 세포는 단백질을 쉼 없이 찍어내고, 어떤 세포는 휴식 중인 상태로 존재한다는 사실이 밝혀졌습니다.[14]
이 기술은 자폐증, 취약 X 증후군처럼 단백질 합성 결함이 원인으로 의심되는 질환들을 연구하는 데 혁신적인 도구가 될 것입니다.
유전자 검사만으로는 알 수 없었던 ‘실제 일하는 뇌세포’의 상태를 비로소 파악할 수 있게 되었기 때문입니다.[14]
참고자료
- In AD Patients, Neurogenesis Stalls. In Superagers It Ramps Up …, https://www.alzforum.org/news/research-news/ad-patients-neurogenesis-stalls-superagers-it-ramps
- Can you grow new brain cells? The debate could reveal the secret of superagers., https://www.nationalgeographic.com/health/article/superager-brain-cells-neurogenesis
- Can you grow new brain cells? | University of Cincinnati, https://www.uc.edu/news/articles/2026/03/n21393541.html
- Show 1464: Can Vaccines Protect the Brain from Dementia? | The …, https://www.peoplespharmacy.com/articles/show-1464-can-vaccines-protect-the-brain-from-dementia
- Astrocytes coordinate fear memories alongside neurons | Journal …, https://www.pnas.org/post/journal-club/astrocytes-coordinate-fear-memories-alongside-neurons
- Scientists discover new gatekeeper cell in the brain | EurekAlert!, https://www.eurekalert.org/news-releases/1115994
- Fremanezumab Reduces Migraine Days in Children and …, https://medicaldialogues.in/pediatrics-neonatology/news/fremanezumab-reduces-migraine-days-in-children-and-adolescents-nejm-165350
- Research Highlights of the Month – October 2025 – eanNews, https://www.eanpages.org/2025/10/07/research-highlights-of-the-month-october-2025/
- Cells, Volume 15, Issue 3 (February-1 2026) – 100 articles – MDPI, https://www.mdpi.com/2073-4409/15/3
- Press Release: Acoziborole Winthrop, developed by DNDi and Sanofi, receives CHMP positive opinion as three-tablet, single-dose treatment for most common form of sleeping sickness, https://www.sanofi.com/en/media-room/press-releases/2026/2026-02-27-10-55-51-3246379
- When a helpful brain signal gets stuck: A new clue in autism biology | EurekAlert!, https://www.eurekalert.org/news-releases/1118754
- Loss of function of the chromatin remodeling gene INO80D leads to neurogenic features of schizophrenia | PNAS, https://www.pnas.org/doi/full/10.1073/pnas.2536039123
- Two New Breakthroughs Advance Neurological Disorders and Cancer Research, https://www.ucsf.edu/news/2026/01/431411/two-new-breakthroughs-advance-neurological-disorders-and-cancer-research
- New technology maps protein production across individual brain cells – News-Medical, https://www.news-medical.net/news/20260218/New-technology-maps-protein-production-across-individual-brain-cells.aspx
- Top 5 AI in Neuroscience Research Trends and Predictions in 2026 – Business 2.0 News, https://business20channel.tv/top-5-ai-in-neuroscience-research-trends-and-predictions-in–12-february-2026
- Evidence for representation of pretend objects by Kanzi, a language trained bonobo, https://research-portal.st-andrews.ac.uk/en/publications/evidence-for-representation-of-pretend-objects-by-kanzi-a-languag/
- Table of Contents — February 25, 2026, 46 (8) | Journal of Neuroscience, https://www.jneurosci.org/content/46/8
- Brain Sci., Volume 16, Issue 2 (February 2026) – 130 articles – MDPI, https://www.mdpi.com/2076-3425/16/2