이번 포스트에서는 2026년 2월 한 달간 발표된 유전체학(Genomics)과 유전체 공학(Genome Engineering) 분야의 최첨단 연구들을 집대성하여 정리했습니다.
이제 우리는 유전체를 단순히 선형적인 ‘정보의 나열’로 보는 시대를 넘어, 고도로 계산된 ‘3차원 건축물’이자 ‘프로그래밍 가능한 코드’로 이해하는 시대에 진입했습니다.
인공지능이 생명의 언어를 해석하는 소식부터, 암의 근원을 파고드는 롱리드 시퀀싱의 정밀함까지 이야기들을 지금 시작합니다.
암 유전체의 새로운 패러다임
L1이 암의 촉발 원인?
인간 유전체의 약 17%를 차지하면서도 오랫동안 ‘쓰레기 DNA’로 무시당해 온 LINE-1(L1) 요소가 암 발생의 초기 핵심 동력이라는 사실이 Science지에 발표되었습니다.
베르나르도 로드리게스-마르틴(Bernardo Rodriguez-Martin) 박사가 주도한 이번 연구는 암세포 내에서 L1이 일으키는 대규모 유전체 재배열의 실체를 낱낱이 파헤쳤습니다. [5, 20]
L1은 스스로를 복제하여 유전체의 다른 위치로 옮겨갈 수 있는 ‘역전사 트랜스포존(Retrotransposon)’입니다.
평소에는 메틸화(Methylation)라는 자물쇠에 잠겨 조용히 지내지만, 암세포의 비정상적인 환경에서는 이 자물쇠가 풀리며 폭주하기 시작합니다.
연구팀은 기존의 짧은 서열 분석법(Short-read)으로는 포착할 수 없었던 복잡한 구조 변화를 관찰하기 위해 롱리드 시퀀싱(Long-read sequencing) 기술을 전격 도입했습니다. [5, 21]
| L1 유발 유전체 변이 유형 | 메커니즘 설명 | 암세포에 미치는 영향 |
|---|---|---|
| 단순 삽입 (Insertion) | L1 사본이 특정 유전자 내부에 끼어듦 | 암 억제 유전자의 기능 파괴 |
| 결손 (Deletion) | L1이 옮겨가는 과정에서 주변 DNA를 삭제 | 대규모 유전 정보 손실 유발 |
| 상호 전좌 (Reciprocal Translocation) | 서로 다른 염색체 조각을 통째로 교환 | 종양 발생의 강력한 드라이버로 작용 |
| 구조적 카오스 | 1/40 확률로 발생하는 대규모 재배열 | 암세포의 전이 및 약물 내성 강화 |
가장 충격적인 발견은 L1의 활동 시기입니다.
연구 결과, L1에 의한 유전체 변이의 무려 65%가 암이 진단되기 수년 전, 심지어 종양이 본격적으로 형성되기 시작하는 초기 단계에서 발생한다는 사실이 확인되었습니다.
이는 L1이 암의 결과물로 나타나는 현상이 아니라, 암이라는 질병을 촉발하는 ‘원인’ 중 하나임을 시사합니다. [20, 22]
역전사 트랜스포존(Retrotransposon)
역전사 트랜스포존(Retrotransposon)은 유전체 내에서 자신의 위치를 복제하여 다른 곳으로 이동시키는 유전 요소로, 소위 “복사해서 붙여넣기(Copy-and-Paste)” 방식으로 작동합니다.
역전사 기전: RNA 중간체를 거치는 ‘복사 후 붙여넣기’ 방식을 사용하므로, 원래 위치의 유전자는 보존되면서 유전체 내 복제본 숫자가 늘어납니다.
분류: 크게 LTR(Long Terminal Repeat) 트랜스포존과 Non-LTR 트랜스포존(LINEs, SINEs)으로 나뉩니다. 인간 유전체의 약 42%가 이 역전사 트랜스포존 유래 서열입니다.
핵심 효소: LINE-1(L1) 요소는 스스로 역전사 효소(Reverse Transcriptase)와 엔도뉴클레아제(Endonuclease)를 암호화하여 이동에 필요한 도구를 직접 생성합니다.
LTR 유형의 유래: LTR 역전사 트랜스포존은 구조적으로 레트로바이러스(Retrovirus)와 거의 동일합니다. 과거에 감염된 바이러스가 생식세포의 유전체에 박힌 뒤, 감염성은 잃고 복제 능력만 남은 ‘내생성 레트로바이러스(ERV)’가 그 기원입니다.
유전적 불안정성: 무분별한 삽입은 정상 유전자를 파괴하여 암(Cancer)이나 희귀 유전병(혈우병 등)을 유발합니다.
노화와 염증: 세포가 노화되면 트랜스포존을 억제하는 기전이 약해집니다. 이때 활성화된 트랜스포존 RNA나 DNA 조각을 세포가 바이러스 감염으로 오인하여 만성 염증 반응(Inflataging)을 일으킨다는 것이 입증되었습니다
원형 DNA
암세포는 일반 세포와 달리 핵 밖을 떠도는 고리 모양의 DNA, 즉 외염색체 원형 DNA(eccDNA)를 다량 보유하고 있습니다.
이 원형 DNA들은 암 유전자를 수백 배로 증폭시키고, 세포 분열 시 무작위로 분배되어 종양의 이질성(Heterogeneity)을 극대화합니다. [23]
2026년 2월, 연구자들은 딥러닝 프레임워크인 DeepECC를 통해 유전체 전체에서 이러한 eccDNA를 식별하고 그 조절 기능을 분석하는 데 성공했습니다.
분석 결과, eccDNA는 단순히 떠도는 쓰레기가 아니라 암세포의 단백질 번역 시스템과 DNA 손상 복구 기작을 장악하는 정교한 조절자로 기능하고 있었습니다. [23]
eccDNA(extrachromosomal circular DNA)
eccDNA(extrachromosomal circular DNA, 염색체 외 원형 DNA)는 최근 암 유전학 및 노화 연구에서 가장 주목받는 주제 중 하나입니다.
일반적인 DNA가 선형(Linear) 형태로 염색체 내에 고정되어 있는 것과 달리, 염색체 밖에서 독립적으로 존재하는 원형의 DNA 조각을 말합니다.
생성 기전 (Chromothripsis): ‘염색체 파쇄’ 현상에 의해 발생한다는 가설이 유력합니다. 염색체가 물리적 스트레스로 인해 조각난 뒤, 이를 복구하는 과정에서 실수로 원형으로 연결되어 eccDNA가 생성된다는 이론입니다.
구조적 특징: 말단(Telomere)이 없는 폐쇄형 원형 구조를 가집니다. 이 구조 덕분에 세포 내의 핵산 분해 효소(Exonuclease)로부터 분해되지 않고 안정적으로 유지됩니다.
높은 유전자 발현: eccDNA는 염색체의 단단한 응축 구조(Heterochromatin)에서 벗어나 있어, 전사 효소가 접근하기 매우 쉽습니다. 따라서 그 안에 포함된 유전자는 일반 유전자보다 훨씬 강력하게 발현됩니다.
불균등 분열 (Random Inheritance): 세포 분열 시 염색체처럼 방추사에 매달려 정확히 반으로 나뉘지 않습니다. 어떤 딸세포는 eccDNA를 몽땅 가져가고, 어떤 세포는 하나도 못 가져가는 ‘무작위 계승’이 일어납니다.
암세포에서의 발견: 암세포에서 특정 암 유전자(Oncogene)가 eccDNA 형태로 복제되어 수백 카피씩 존재한다는 사실이 밝혀졌습니다. 이는 암의 빠른 증식과 약물 내성의 핵심 기전입니다.
정밀 유전체 공학: 더 작고 강력한 가위와 유전자 드라이브
크기는 작지만 효율은 90%: 차세대 가위 TnpB
CRISPR/Cas9은 세상을 바꿨지만, 1,300개가 넘는 아미노산으로 이루어진 Cas9의 거대한 몸집은 늘 걸림돌이었습니다.
바이러스에 실어 세포 내로 전달하기에는 너무 무거웠기 때문입니다. Nature Plants에 발표된 UC 데이비스와 IGI의 공동 연구는 이 문제를 TnpB라는 ‘미니 효소’로 해결했습니다. [26]
TnpB는 박테리아의 전이 인자(Transposon)와 연관된 효소로, Cas9의 조상 격인 존재입니다.
크기는 Cas9의 3분의 1 수준인 400개 아미노산에 불과하지만, 연구팀이 개량한 ‘eTnpBc’ 버전은 담배 식물 실험에서 90% 이상의 경이로운 유전자 교정 효율을 보여주었습니다. [26, 27]
TnpB
진화적 기원: TnpB는 CRISPR-Cas12 단백질의 직계 조상입니다. 즉, 박테리아의 면역 체계인 CRISPR 시스템이 형성되기 전부터 존재했던 원시적인 형태의 핵산 분해 효소입니다.
구조적 특징: Cas9이나 Cas12에 비해 크기가 매우 작습니다(약 350~450개 아미노산). 이는 세포 내 전달(Delivery)이 용이하다는 공학적 장점을 가집니다.
OMEGA 시스템: TnpB는 OMEGA(Obligate Mobile Element-guided Activity) 시스템의 핵심 요소입니다. 이 시스템은 RNA를 가이드로 삼아 DNA를 절단하는 기전을 가집니다.
reRNA의 사용: Cas9이 gRNA(guide RNA)를 사용하는 것처럼, TnpB는 reRNA(Right-end-associated RNA)라고 불리는 짧은 RNA를 사용하여 표적 DNA 서열을 찾아갑니다.
TnpB가 특정 DNA를 찾아가서 자르는 과정은 다음과 같은 단계를 거칩니다.
- 복합체 형성: TnpB 단백질이 전이인자의 끝부분에서 전사된 reRNA와 결합하여 활성 복합체를 형성합니다.
- 표적 탐색 (TAM 인식): Cas9이 PAM(Protospacer Adjacent Motif) 서열을 인식하듯, TnpB는 TAM(Transposon-associated Motif)이라는 짧은 염기서열을 인식하여 DNA에 달라붙습니다.
- DNA 절단: reRNA가 표적 DNA 서열과 상보적으로 결합하면, TnpB의 RuvC 도메인(핵산 분해 활성 부위)이 작동하여 DNA 이중 가닥을 절단합니다.
논쟁
최근 연구(특히 펑 장 교수팀의 연구)에서는 TnpB를 엔지니어링하여 Cas9 수준의 정확도를 확보할 수 있음을 보여주었으나, 자연 상태의 TnpB가 가진 오프-타겟(Off-target, 비표적 절단) 위험성은 여전히 면밀히 검토되어야 할 대상입니다.
“작은 크기가 반드시 낮은 정확도로 이어지는가”에 대해 논쟁 중입니다.
세계 최초의 Trimodal 지도: scHiCAR
세포의 상태를 완벽하게 이해하려면 세 가지 질문에 동시에 답해야 합니다.
“지금 무슨 일이 일어나는가(전사체)”, “왜 일어나는가(후성유전체)”, “어디서 일어나는가(3D 구조)”.
2026년 2월 Nature Biotechnology에 발표된 scHiCAR 기술은 이 세 가지 데이터를 단일 세포 수준에서 동시에 읽어내는 쾌거를 이루었습니다. [29, 30]
기존에는 이 정보를 얻기 위해 서로 다른 세포들로부터 데이터를 얻어 사후에 짜맞추는 방식을 썼는데, 이 과정에서 미세한 변화들이 왜곡되거나 사라지는 문제가 있었습니다.
scHiCAR는 AI 기반의 통합 분석 알고리즘을 도입하여 정확도를 획기적으로 높였으며, 분석 비용을 세포당 약 50원($0.04) 수준으로 낮추어 대규모 분석의 길을 열었습니다. [29, 30]
| scHiCAR 분석 데이터 레이어 | 생물학적 의미 | 질병 연구의 적용 |
|---|---|---|
| 전사체 (RNA-seq) | 현재 단백질 생산 설계도 발현량 | 질병 특이적 유전자 활성 포착 |
| 후성유전체 (ATAC-seq) | 유전체 부위의 개방성/접근성 | 발현 잠재력 및 조절 부위 식별 |
| 3D 유전체 (Hi-C) | DNA 간의 물리적 거리와 루프 | 강화자 하이재킹(Enhancer Hijacking) 탐지 |
연구진은 이 기술을 쥐의 뇌 조직과 근육 재생 과정에 적용하여 160만 개 세포의 고해상도 지도를 작성했습니다.
특히 근육 줄기세포가 재생되는 과정에서 DNA의 3차원 구조가 어떻게 실시간으로 변하며 세포의 운명을 결정하는지를 세계 최초로 포착해 냈습니다. [29, 30]
비부호화 DNA: 98%의 ‘암흑 물질’이 주도하는 유전학
질병의 진짜 원인은 유전자 밖에 있다: 대규모 변이 지도의 완성
인간 유전체의 98%는 단백질을 직접 만들지 않는 ‘비부호화 영역(Non-coding DNA)’입니다.
과거에는 이를 진화의 찌꺼기로 여겼지만, Broad Institute와 Yale 대학교의 연구는 이곳이 우리 건강을 좌우하는 ‘진짜 컨트롤 타워’임을 증명했습니다. [32]
연구팀은 대규모 병렬 리포터 분석(MPRA) 기술을 사용하여 질병과 연관된 것으로 의심되는 220,000개 이상의 유전적 변이를 다섯 종류의 인간 세포에서 동시에 테스트했습니다.
그 결과, 혈압, 콜레스테롤 수치, 혈당 조절에 결정적인 영향을 미치는 13,000개 이상의 핵심 변이를 찾아냈습니다. [32]
| 질환 관련 지표 | 발견된 변이의 특성 | 혁신적인 통찰 |
|---|---|---|
| LDL 콜레스테롤 | 특정 변이 쌍이 시너지를 냄 | ‘부분의 합보다 큰’ 유전적 상호작용 확인 |
| 혈당 조절 | 비유럽계 인구 특이적 변이 발견 | 유전체 연구의 인종적 형평성 제고 |
| 발달 장애 (ESS2) | 변이 결합 시 전사 효율 극대화 | 단일 변이 분석의 한계 극복 |
| 비부호화 영역 | 전체 변이의 90% 이상 집중 | 조절 문법(Regulatory Grammar)의 중요성 |
특히 변이들이 단독으로 작용할 때보다 특정한 조합을 이룰 때 그 영향력이 증폭된다는 ‘유전적 에피스타시스(Epistasis)’ 현상이 변이의 11%에서 관찰되었습니다.
이는 미래의 질병 예측 모델이 단순한 합산이 아니라 복잡한 상관관계를 고려한 AI 기반의 모델이어야 함을 강력하게 시사합니다. [32]
HSat3 위성 DNA
스탠퍼드 대학교의 니콜라스 알테모즈(Nicolas Altemose) 교수팀은 유전체에서 가장 미스테리한 영역 중 하나인 ‘위성 DNA(Satellite DNA)’의 비밀을 풀었습니다.
HSat3라고 불리는 이 고도로 반복되는 서열들은 오랫동안 유전적 잡음으로 여겨져 왔습니다. [6]
하지만 롱리드 시퀀싱과 초고해상도 현미경 분석 결과, HSat3는 세포의 성장을 조절하는 ‘거대한 스펀지’ 역할을 하고 있었습니다.
세포가 성장에 필요한 단백질을 만드는 공장인 리보솜을 돌리기 위해 TEAD라는 핵심 전사 인자를 핵 내의 특정 지점(인, Nucleolus)으로 끌어모으고 집중시키는 역할을 수행하는 것입니다.
만약 HSat3를 인위적으로 억제하면 TEAD가 흩어지고 리보솜 생산이 급락하며 세포 성장이 멈춥니다.
이는 암세포의 무분별한 증식을 막는 새로운 치료 타겟으로 위성 DNA가 부상할 수 있음을 보여주는 획기적인 연구입니다. [6, 33]
HSat3
반복 서열 구조: 주로 GGAAT라는 5개 염기쌍(Pentamer)이 수천, 수만 번 반복된 형태입니다.
위치: 주로 9번 염색체의 거대한 이질염색질(Heterochromatin) 부위에 집중되어 있으며, 1번, Y번 염색체 등에도 분포합니다.
스트레스 유도 전사: 평상시에는 ‘침묵’ 상태(사일런싱)를 유지하지만, 열충격(Heat Shock)과 같은 세포 스트레스가 발생하면 급격히 RNA로 전사됩니다.
nSB(Nuclear Stress Bodies) 형성: 스트레스 상황에서 전사된 HSat3 RNA는 핵 내의 특정 단백질(예: HSF1, SAFB)을 끌어모아 핵 스트레스 체(nSB)라는 독특한 막 없는 구조체를 형성합니다.
비부호화 RNA (lncRNA)
HSat3 DNA가 전사되어 만들어진 RNA는 단백질로 번역(Translation)되지 않습니다.
이를 긴 비부호화 RNA(long non-coding RNA, lncRNA)라고 부릅니다.
HSat3에는‘단백질의 아미노산 서열’에 대한 정보는 없지만, ‘핵 내 구조물을 형성하고 특정 단백질을 끌어당기는 물리적/화학적 정보’는 담겨 있습니다.
3D 게놈 아키텍처: Pico-C 기술의 혁명
수정란이라는 단 하나의 세포가 어떻게 그 복잡한 생명체로 자라날까요?
오랫동안 과학자들은 배아 초기 단계의 DNA는 마치 엉킨 실타래처럼 무질서한 상태로 있다가, 특정 시점(ZGA)에 도달해서야 비로소 정돈된다고 생각했습니다.
하지만 2026년 2월 Nature Genetics와 Nature Cell Biology는 이 ‘백지설’을 정면으로 반박하는 결과를 발표했습니다. [17, 18, 19]
Pico-C: 유전자의 입체 설계도 확인
후안마 바케리자스(Juanma Vaquerizas) 교수팀은 단 수천 개의 세포만으로도 DNA의 3차원 구조를 정밀하게 분석할 수 있는 ‘Pico-C’ 기술을 개발했습니다.
기존 기술(Hi-C)은 수백만 개의 세포가 필요했기에 배아 초기 단계를 분석하는 것이 거의 불가능했습니다. [19]
이 기술로 초파리 배아를 관찰한 결과, 유전자가 본격적으로 켜지기도 전부터 DNA는 이미 정교한 ‘비계(Scaffolding)’를 쌓고 있었습니다.
특정 유전자를 켜기 위한 스위치와 조절 장치가 미리 고리(Loop)를 만들어 서로를 마주 보고 대기하고 있었던 것이죠.
이 발견은 생명의 설계도가 우리가 생각한 것보다 훨씬 일찍, 그리고 훨씬 입체적으로 준비된다는 사실을 보여줍니다. [18, 19, 20]
Hi-C
Hi-C 기술은 세포 핵 안에서 실타래처럼 복잡하게 꼬여 있는 DNA의 3차원 구조(3D Genome Architecture)를 전장 유전체(Genome-wide) 수준에서 파악하기 위한 혁신적인 분석법입니다.
동작 원리
Hi-C의 핵심 아이디어는 “3차원 공간상에서 물리적으로 가까이 있는 DNA 조각들을 서로 붙여버린 뒤 서열을 읽는 것”입니다.
실험 단계
- 가교 결합 (Cross-linking): 포름알데히드 등을 사용하여 물리적으로 가까운 DNA와 단백질들을 화학적으로 고정합니다. (이때 선형 서열상으로는 멀리 있어도 공간적으로 가까우면 함께 묶입니다.)
- 제한효소 절단 (Digestion): DNA를 특정 서열 부위에서 자릅니다.
- 말단 표지 (Biotin Fill-in): 잘린 단면을 비오틴(Biotin)이라는 물질로 표지합니다.
- 근접 결합 (Proximity Ligation): 아주 묽은 농도에서 다시 이어 붙입니다. 이때 ‘가까이 묶여 있던 조각들끼리’ 만날 확률이 높으므로, 원래 공간적으로 이웃했던 두 서열이 하나로 합쳐진 키메라(Chimeric) DNA가 생성됩니다.
- 시퀀싱 및 분석: 비오틴을 이용해 키메라 DNA만 정제한 후 차세대 염기서열 분석(NGS)을 수행합니다.
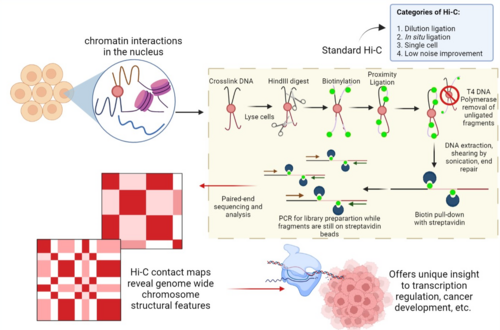
주요 연구 및 활용 분야
암 및 유전 질환 연구: 암세포에서 일어나는 염색체 전좌(Translocation)나 구조적 변이가 3D 구조를 어떻게 파괴하여 비정상적인 유전자 발현을 일으키는지 연구합니다.
유전자 조절 기전 연구: 선형 서열상으로는 아주 멀리 떨어진 ‘인핸서’가 어떻게 특정 유전자의 ‘프로모터’와 만나 스위치를 켜는지 밝혀냅니다.
유전체 조립 (Genome Assembly): 조각난 DNA 서열들이 실제 염색체상에서 어떤 순서로 배치되어야 하는지 알려주는 ‘지지도’ 역할을 합니다.
설계도가 무너지면 몸은 “바이러스가 침입했다”고 착각한다
더욱 충격적인 것은 Nature Cell Biology에 실린 동반 연구입니다.
연구팀이 유전자 구조를 지탱하는 핵심 단백질(LBR, LAP2)을 제거하여 이 3D 비계를 무너뜨려 보았습니다.
그러자 세포 내의 면역 센서인 ‘cGAS-STING’ 경로가 즉각 가동되었습니다. [17, 19]
이 센서는 보통 세포질로 삐져나온 바이러스 DNA를 감지해 염증 반응을 일으키는 녀석인데, 유전자 구조가 무너지면서 삐져나온 우리 몸의 DNA를 바이러스로 착각한 것입니다.
즉, 게놈의 물리적 구조가 변하는 것만으로도 우리 몸은 스스로를 공격하는 ‘자가면역 질환’ 상태에 빠질 수 있다는 메커니즘이 처음으로 증명된 것입니다.
이는 암이나 노화 과정에서 발생하는 만성 염증의 근본 원인을 설명하는 강력한 이론이 될 것입니다. [19, 20]
LBR, LAP2, 핵막과 DNA를 잇는 다리
이 두 단백질은 내핵막(Inner Nuclear Membrane, INM)에 박혀 있는 단백질들입니다.
역할: 라민 A(Lamin A) 및 BAF라는 단백질과 결합하여 DNA를 핵막에 고정합니다. 특히 세포 분열 후 핵막이 다시 만들어질 때 염색체를 감싸는 데 핵심적인 역할을 합니다.
LBR (Lamin B Receptor):
위치: 내핵막에 고정되어 있습니다.
역할: 핵 내부의 라민 B(Lamin B) 단백질 및 HP1(Heterochromatin Protein 1)과 결합합니다. 이를 통해 유전정보를 읽기 어렵게 뭉쳐놓은 ‘외질염색질(Heterochromatin)’을 핵막 근처에 붙잡아 둡니다.
LAP2 (Lamina-Associated Polypeptide 2):
위치: 역시 내핵막에 존재하는 단백질 가족(Family)입니다.
DNA와 결합하는 여러 단백질들
히스톤은 DNA를 감싸서 보관하는 ‘포장재’라면, 다른 단백질들은 다양한 목적(수리, 복제, 구조 유지)으로 DNA와 결합합니다.
효소: DNA 중합효소(Polymerase), 헬리케이스(Helicase) – 복제와 전사를 수행합니다.
구조 단백질: 코히신(Cohesin), 콘덴신(Condensin) – 염색체의 형태를 유지합니다.
조절 단백질: 전사 인자(Transcription Factors) – 특정 유전자를 켜고 끕니다.
참고자료
- New technology reveals hidden DNA scaffolding built before life ‘switches on’ | EurekAlert!, https://www.eurekalert.org/news-releases/1117395
- Stunning 3D maps reveal DNA is structured before life “switches on” | ScienceDaily, https://www.sciencedaily.com/releases/2026/02/260227061824.htm
- New Technology Reveals Hidden DNA Scaffolding Built Before Life “Switches On”, https://bioquicknews.com/new-technology-reveals-hidden-dna-scaffolding-built-before-life-switches-on/
- With Evo 2, AI Can Model And Design The Genetic Code For All Domains Of Life, https://astrobiology.com/2026/03/with-evo-2-ai-can-model-and-design-the-genetic-code-for-all-domains-of-life.html
- Jumping ‘DNA parasites’ linked to early stages of tumour … – CRG, https://www.crg.eu/en/news/jumping-dna-parasites-linked-early-stages-tumour-formation
- Mystery solved of repetitive DNA sequences’ role in cell growth – Stanford Medicine Magazine, https://stanmed.stanford.edu/repetitive-dna-control-cell-division/
- From The Medical Research Council (MRC) – UKRI [ENG] Via SciTechDaily: “Scientists Discover DNA Is Already Organized Before Life Switches On” – sciencesprings, https://sciencesprings.wordpress.com/2026/03/01/from-the-medical-research-council-mrc-ukri-eng-via-scitechdaily-scientists-discover-dna-is-already-organized-before-life-switches-on/
- Pico-C Technology Reveals Genome Structure Before Activation – DistilINFO, https://distilinfo.com/2026/02/25/pico-c-technology-reveals-genome-structure-before-activation/
- New Tech Unveils Pre-Life DNA Scaffolding | Mirage News, https://www.miragenews.com/new-tech-unveils-pre-life-dna-scaffolding-1625389/
- New technology reveals hidden DNA scaffolding built before life …, https://lms.mrc.ac.uk/new-technology-reveals-hidden-dna-scaffolding-built-before-life-switches-on/
- New Pico C technology maps genome structure before activation – News-Medical, https://www.news-medical.net/news/20260224/New-Pico-C-technology-maps-genome-structure-before-activation.aspx
- Imaging Technique Reveals DNA’s Hidden Shape in the Earliest of Embryos, https://www.discovermagazine.com/imaging-technique-reveals-dna-s-hidden-shape-in-the-earliest-of-embryos-48747
- (PDF) Three-dimensional genome reorganization foreshadows zygotic genome activation in Drosophila – ResearchGate, https://www.researchgate.net/publication/401159549_Three-dimensional_genome_reorganization_foreshadows_zygotic_genome_activation_in_Drosophila
- With Evo 2, AI can model and design the genetic code for all domains of life | EurekAlert!, https://www.eurekalert.org/news-releases/1118060
- Evo 2 AI Models Genetic Code for All Life Domains – Berkeley Today, https://nationaltoday.com/us/ca/berkeley/news/2026/03/05/evo-2-ai-models-genetic-code-for-all-life-domains/
- AI trained on 9 trillion DNA letters predicts harmful mutations and designs new genomes, https://www.news-medical.net/news/20260305/AI-trained-on-9-trillion-DNA-letters-predicts-harmful-mutations-and-designs-new-genomes.aspx
- Genome modelling and design across all domains of life with Evo 2 – ResearchGate, https://www.researchgate.net/publication/401577941_Genome_modelling_and_design_across_all_domains_of_life_with_Evo_2
- AI Takes Over Life Itself: Meet Evo-2, The Artificial Intelligence That Can Write DNA From Scratch! – BioTecNika, https://www.biotecnika.org/2025/02/evo-2-ai-writing-dna-genetic-codes/
- New AI breakthrough can model and design genetic code across all domains of life, https://engineering.berkeley.edu/news/2025/02/new-ai-breakthrough-can-model-and-design-genetic-code-across-all-domains-of-life/
- Jumping DNA fragments found to destabilize cancer genome – News-Medical, https://www.news-medical.net/news/20260226/Jumping-DNA-fragments-found-to-destabilize-cancer-genome.aspx
- Jumping ‘DNA parasites’ linked to early stages of tumour formation – EurekAlert!, https://www.eurekalert.org/news-releases/1117270
- Jumping DNA Parasites Implicated in Early Tumor Development – BIOENGINEER.ORG, https://bioengineer.org/jumping-dna-parasites-implicated-in-early-tumor-development/
- DeepECC: a deep learning framework for genome-wide identification and analysis of human cancer eccDNAs | Nucleic Acids Research | Oxford Academic, https://academic.oup.com/nar/article-abstract/doi/10.1093/nar/gkag198/8506940
- Cells, Volume 15, Issue 3 (February-1 2026) – 100 articles – MDPI, https://www.mdpi.com/2073-4409/15/3
- Tumor Genomics and Liquid Biopsy in Cancer Biology: From Static Snapshots to Dynamic Measurements – MDPI, https://www.mdpi.com/2218-273X/16/3/384
- Pint-Sized Gene Editor Could Expand Precision Breeding in Plants, https://innovativegenomics.org/news/pint-sized-gene-editor-could-expand-precision-breeding-in-plants/
- Advancing Genome Engineering – Innovative Genomics Institute (IGI), https://innovativegenomics.org/programs/advancing-genome-engineering/
- Breakthrough CRISPR system could reverse antibiotic resistance crisis – ScienceDaily, https://www.sciencedaily.com/releases/2026/02/260217005717.htm
- Simultaneous decoding of genetic maps inside cells. . . A game changer for understanding complex human diseases | EurekAlert!, https://www.eurekalert.org/news-releases/1119015
- Breakthrough in Genetic Maps Decoding for Disease Insight | Mirage News, https://www.miragenews.com/breakthrough-in-genetic-maps-decoding-for-1632516/
- Information Geometry Reconciles Discrete and Continuous Variation in Single-Cell and Spatial Transcriptomic Analysis | bioRxiv, https://www.biorxiv.org/content/10.64898/2026.02.25.707866v1
- Scientists sharpen genetic maps to help pinpoint DNA changes that influence human health traits and disease risk | Broad Institute, https://www.broadinstitute.org/news/scientists-sharpen-genetic-maps-help-pinpoint-dna-changes-influence-human-health-traits-and
- Molecular & Structural Biology – News-Medical.Net, https://www.news-medical.net/category/Molecular-Structural-Biology.aspx
- Reproductive Tech That Promises Smart Babies Is Peddling Soft Eugenics | Truthout, https://truthout.org/articles/reproductive-tech-that-promises-smart-babies-is-peddling-soft-eugenics/
- Human Genome Editing: Science, Ethics, and Governance | The National Academies Press, https://www.nationalacademies.org/publications/24623
- Genome editing: the dynamics of continuity, convergence, and change in the engineering of life – Taylor & Francis, https://www.tandfonline.com/doi/full/10.1080/14636778.2020.1730166
- Illumina and the San Diego Zoo Wildlife Alliance partner to sequence the Frozen Zoo®, supporting critical conservation genetics efforts globally, https://www.illumina.com/company/news-center/press-releases/press-release-details.html?newsid=ccb9e4de-b781-4645-a540-f471c780d248
- Two New Breakthroughs Advance Neurological Disorders and Cancer Research, https://www.ucsf.edu/news/2026/01/431411/two-new-breakthroughs-advance-neurological-disorders-and-cancer-research
- Deep Learning-Enabled Multi-Omics Integration: A New Frontier in Precise Drug Target Discovery – MDPI, https://www.mdpi.com/2079-7737/15/5/410