지구상에 존재하는 수조 개의 세포는 매 순간 끊임없이 대화하고 있다는 사실, 알고 계셨나요?
마치 우리가 스마트폰으로 메시지를 주고받으며 정보를 교환하고 사회를 유지하듯, 우리 몸속 세포들도 ‘세포 신호전달(Cell Signaling)’이라는 정교한 통신망을 통해 생명을 유지합니다. 하지만 가끔 이 통신망에 혼선이 생기거나, 암세포처럼 교묘하게 보안을 뚫고 가짜 정보를 퍼뜨리는 녀석들이 나타나면 우리 몸은 병에 걸리게 됩니다.
2026년 2월, 이 복잡한 통신 시스템의 암호를 해독한 기념비적인 연구들을 쏟아냈습니다.
이번 포스트에서는 암세포가 굶주림을 버티는 비상식량의 비밀부터, 우리 몸이 늙어가며 스스로 공장을 리모델링하는 이유, 그리고 생명이 시작되는 찰나의 정교한 설계도까지, 최신 소식들을 하나하나 파헤쳐 보겠습니다.
항암 치료의 패러다임을 바꿀 대사 신호의 대발견: 비오틴과 FBXW7
암세포는 흔히 ‘글루타민 중독(Glutamine Addiction)’에 빠져 있다고 표현됩니다.
글루타민은 단백질과 DNA의 기초 블록을 제공하는 필수 아미노산인데, 암세포는 폭발적인 성장을 위해 이 글루타민을 엄청나게 먹어치우죠.
그래서 그동안 많은 항암제가 글루타민 대사를 차단하는 방식을 썼지만, 이상하게도 결과는 늘 신통치 않았습니다.
암세포가 이 포위망을 뚫고 살아남는 ‘대사 우회로’가 있었기 때문인데, 2026년 2월 Molecular Cell에 그 비밀이 공개되었습니다. [5, 6, 7]
비타민 B7(비오틴), 암세포에게 ‘대사 허가증’을 내주다
로잔 대학교(Unil)의 알렉시 주르댕(Alexis Jourdain) 교수팀과 미레암 리시(Miriam Lisci) 박사는 암세포가 글루타민이 부족한 척박한 환경에서도 당당히 성장을 이어가는 메커니즘을 규명했습니다.
연구팀은 탄소가 풍부한 분자인 ‘피루브산(Pyruvate)’이 글루타민의 역할을 대신할 수 있다는 점에 주목했습니다. [5, 6, 7]
실험 결과, 이 과정에는 미토콘드리아 효소인 ‘피루브산 카복실화 효소(Pyruvate Carboxylase)’가 핵심적인 역할을 합니다.
그런데 이 효소가 작동하려면 반드시 필요한 ‘열쇠’가 있는데, 그것이 바로 비타민 B7으로 알려진 ‘비오틴(B7)’입니다.
비오틴이 없는 환경에서는 이 효소가 비활성화되어 암세포가 우회로를 찾지 못하고 성장이 멈추지만, 비오틴이 충분하면 암세포는 피루브산을 이용해 에너지 회로(TCA cycle)를 돌리며 글루타민 부족을 비웃듯 자라납니다.
연구팀은 이를 비오틴이 암세포에게 주는 ‘대사 허가증(Metabolic License)’이라고 명명했습니다. [6, 7, 8]
FBXW7 유전자 변이가 만드는 글루타민 의존성
더욱 흥미로운 점은 다양한 암종에서 빈번하게 발생하는 ‘FBXW7’ 유전자의 돌연변이와 이 대사 경로의 상관관계입니다.
FBXW7은 본래 종양 억제 유전자로, 필요 없는 단백질을 분해하도록 유도하는 역할을 합니다. 연구팀은 이 유전자에 변이가 생기면 피루브산 카복실화 효소의 양이 줄어들거나 기능이 상실된다는 것을 발견했습니다. [6, 8]
즉, FBXW7 변이가 있는 암세포는 비오틴이 있어도 피루브산을 제대로 쓰지 못하고, 오로지 글루타민에만 100% 의존하는 진정한 ‘글루타민 중독’ 상태가 됩니다.
이는 환자의 유전 정보를 통해 어떤 환자에게 글루타민 차단제가 효과적일지 미리 알 수 있는 강력한 지표가 됩니다.
반대로 FBXW7이 정상인 환자는 글루타민만 막아서는 안 되며, 비오틴 대사까지 동시에 타격해야 한다는 전략적 통찰을 제공합니다. [6, 7]
| 대사 요소 | 일반적인 역할 | 암세포에서의 변칙적 활용 | 관련 연구 결과 |
|---|---|---|---|
| 글루타민 | 단백질/DNA 합성 재료 | 폭발적 성장을 위한 주 에너지원 | 글루타민 중독 치료의 타겟 [9] |
| 비오틴(B7) | 필수 비타민, 조효소 | 피루브산 우회로를 여는 “허가증” | 부족 시 우회로 차단 [7] |
| FBXW7 | 종양 억제, 단백질 분해 조절 | 변이 시 피루브산 이용 능력 상실 | 특정 암세포의 아킬레스건 [6] |
| 피루브산 | 당분해 과정의 최종 산물 | TCA 회로를 보충하는 비상 연료 | 비오틴-PC 효소 시스템 활용 [8] |
[알기 쉬운 개념] TCA 회로에서 pyruvate와 비오틴
생화학 시간에 배우는 TCA 회로는 세포의 에너지 공장입니다.
보통 아세틸-CoA(Acetyl−CoA)가 회로에 들어가면서 시작되지만, 물질을 합성하느라 회로의 중간 산물들이 자꾸 빠져나가면 공장이 멈출 수 있습니다.
이때 Pyruvate에 CO2를 붙여 Oxaloacetate를 직접 보충해주는 효소가 바로 피루브산 카복실화 효소(PC)입니다.
이 반응을 ‘보충 반응’이라고 부르며, 암세포는 이 반응을 극대화하여 글루타민 차단이라는 극한 상황을 견뎌냅니다.
비오틴은 이 PC 효소의 활성 부위에 결합하여 CO2를 전달하는 셔틀 역할을 수행합니다. [6, 8]
생명의 시작과 면역의 알람, 3D 게놈 아키텍처: Pico-C 기술의 혁명
수정란이라는 단 하나의 세포가 어떻게 그 복잡한 생명체로 자라날까요?
오랫동안 과학자들은 배아 초기 단계의 DNA는 마치 엉킨 실타래처럼 무질서한 상태로 있다가, 특정 시점(ZGA)에 도달해서야 비로소 정돈된다고 생각했습니다.
하지만 2026년 2월 Nature Genetics와 Nature Cell Biology는 이 ‘백지설’을 정면으로 반박하는 결과를 발표했습니다. [17, 18, 19]
Pico-C: 유전자의 입체 설계도를 훔쳐보다
후안마 바케리자스(Juanma Vaquerizas) 교수팀은 단 수천 개의 세포만으로도 DNA의 3차원 구조를 정밀하게 분석할 수 있는 ‘Pico-C’ 기술을 개발했습니다.
기존 기술(Hi-C)은 수백만 개의 세포가 필요했기에 배아 초기 단계를 분석하는 것이 거의 불가능했습니다. [19]
이 기술로 초파리 배아를 관찰한 결과, 유전자가 본격적으로 켜지기도 전부터 DNA는 이미 정교한 ‘비계(Scaffolding)’를 쌓고 있었습니다.
특정 유전자를 켜기 위한 스위치와 조절 장치가 미리 고리(Loop)를 만들어 서로를 마주 보고 대기하고 있었던 것이죠.
이 발견은 생명의 설계도가 우리가 생각한 것보다 훨씬 일찍, 그리고 훨씬 입체적으로 준비된다는 사실을 보여줍니다. [18, 19, 20]
알기 쉬운 개념: Hi-C
Hi-C 기술은 세포 핵 안에서 실타래처럼 복잡하게 꼬여 있는 DNA의 3차원 구조(3D Genome Architecture)를 전장 유전체(Genome-wide) 수준에서 파악하기 위한 혁신적인 분석법입니다.
동작 원리
Hi-C의 핵심 아이디어는 “3차원 공간상에서 물리적으로 가까이 있는 DNA 조각들을 서로 붙여버린 뒤 서열을 읽는 것”입니다.
실험 단계
- 가교 결합 (Cross-linking): 포름알데히드 등을 사용하여 물리적으로 가까운 DNA와 단백질들을 화학적으로 고정합니다. (이때 선형 서열상으로는 멀리 있어도 공간적으로 가까우면 함께 묶입니다.)
- 제한효소 절단 (Digestion): DNA를 특정 서열 부위에서 자릅니다.
- 말단 표지 (Biotin Fill-in): 잘린 단면을 비오틴(Biotin)이라는 물질로 표지합니다.
- 근접 결합 (Proximity Ligation): 아주 묽은 농도에서 다시 이어 붙입니다. 이때 ‘가까이 묶여 있던 조각들끼리’ 만날 확률이 높으므로, 원래 공간적으로 이웃했던 두 서열이 하나로 합쳐진 키메라(Chimeric) DNA가 생성됩니다.
- 시퀀싱 및 분석: 비오틴을 이용해 키메라 DNA만 정제한 후 차세대 염기서열 분석(NGS)을 수행합니다.
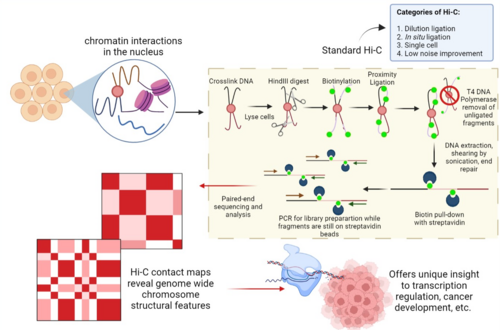
주요 연구 및 활용 분야
암 및 유전 질환 연구: 암세포에서 일어나는 염색체 전좌(Translocation)나 구조적 변이가 3D 구조를 어떻게 파괴하여 비정상적인 유전자 발현을 일으키는지 연구합니다.
유전자 조절 기전 연구: 선형 서열상으로는 아주 멀리 떨어진 ‘인핸서’가 어떻게 특정 유전자의 ‘프로모터’와 만나 스위치를 켜는지 밝혀냅니다.
유전체 조립 (Genome Assembly): 조각난 DNA 서열들이 실제 염색체상에서 어떤 순서로 배치되어야 하는지 알려주는 ‘지지도’ 역할을 합니다.
설계도가 무너지면 몸은 “바이러스가 침입했다”고 착각한다
더욱 충격적인 것은 Nature Cell Biology에 실린 동반 연구입니다.
연구팀이 유전자 구조를 지탱하는 핵심 단백질(LBR, LAP2)을 제거하여 이 3D 비계를 무너뜨려 보았습니다.
그러자 세포 내의 면역 센서인 ‘cGAS-STING’ 경로가 즉각 가동되었습니다. [17, 19]
이 센서는 보통 세포질로 삐져나온 바이러스 DNA를 감지해 염증 반응을 일으키는 녀석인데, 유전자 구조가 무너지면서 삐져나온 우리 몸의 DNA를 바이러스로 착각한 것입니다.
즉, 게놈의 물리적 구조가 변하는 것만으로도 우리 몸은 스스로를 공격하는 ‘자가면역 질환’ 상태에 빠질 수 있다는 메커니즘이 처음으로 증명된 것입니다.
이는 암이나 노화 과정에서 발생하는 만성 염증의 근본 원인을 설명하는 강력한 이론이 될 것입니다. [19, 20]
알기 쉬운 개념: LBR, LAP2, 핵막과 DNA를 잇는 다리
이 두 단백질은 내핵막(Inner Nuclear Membrane, INM)에 박혀 있는 단백질들입니다.
역할: 라민 A(Lamin A) 및 BAF라는 단백질과 결합하여 DNA를 핵막에 고정합니다. 특히 세포 분열 후 핵막이 다시 만들어질 때 염색체를 감싸는 데 핵심적인 역할을 합니다.
LBR (Lamin B Receptor):
위치: 내핵막에 고정되어 있습니다.
역할: 핵 내부의 라민 B(Lamin B) 단백질 및 HP1(Heterochromatin Protein 1)과 결합합니다. 이를 통해 유전정보를 읽기 어렵게 뭉쳐놓은 ‘외질염색질(Heterochromatin)’을 핵막 근처에 붙잡아 둡니다.
LAP2 (Lamina-Associated Polypeptide 2):
위치: 역시 내핵막에 존재하는 단백질 가족(Family)입니다.
알기 쉬운 개념: DNA와 결합하는 여러 단백질들
히스톤은 DNA를 감싸서 보관하는 ‘포장재’라면, 다른 단백질들은 다양한 목적(수리, 복제, 구조 유지)으로 DNA와 결합합니다.
효소: DNA 중합효소(Polymerase), 헬리케이스(Helicase) – 복제와 전사를 수행합니다.
구조 단백질: 코히신(Cohesin), 콘덴신(Condensin) – 염색체의 형태를 유지합니다.
조절 단백질: 전사 인자(Transcription Factors) – 특정 유전자를 켜고 끕니다.
암과 신경의 ‘위험한 동거’를 끊어내는 법: 췌장암의 신경 포섭
췌장암은 5년 생존율이 매우 낮아 ‘암 중의 암’이라 불립니다.
최근 연구들은 췌장암세포가 단순히 혼자 자라는 것이 아니라, 우리 몸의 신경계를 교묘하게 이용한다는 사실을 밝혀냈습니다.
2026년 2월 Science와 Cancer Discovery는 이 사악한 파트너십의 실체를 낱낱이 공개했습니다. [21, 22, 23]
신경을 유혹하는 암의 ‘미인계’
콜드 스프링 하버 연구소(CSHL)의 제레미 니그리(Jeremy Nigri) 박사는 췌장암 조직 내부에 엄청나게 빽빽한 신경망이 형성되어 있다는 것을 3D 이미징 기술로 확인했습니다.
이전에는 신경이 암세포를 따라가는 수동적인 존재로 보였지만, 이번 연구는 암 주변의 섬유아세포(myCAF)가 특정 신호를 보내 주변 신경을 적극적으로 유인(Recruitment)한다는 것을 밝혀냈습니다. [21, 23]
노르에피네프린과 칼슘 스파이크으로 성장하는 암
일단 암 조직으로 들어온 신경은 ‘노르에피네프린’이라는 신경전달물질을 뿌립니다.
이 물질은 myCAF 표면의 수용체에 결합하여 세포 내 칼슘 농도를 폭발적으로 높이는 ‘칼슘 스파이크’를 유도합니다.
이 신호를 받은 myCAF는 더욱 악독하게 변하여 암세포의 성장을 돕고, 다시 더 많은 신경을 불러모으는 신호를 내보냅니다. [21, 23]
연구팀이 신경 독소를 사용해 이 교감신경 신호를 끊어버리자, 놀랍게도 종양의 크기가 50%나 줄어들었습니다.
현재 고혈압 치료제로 사용 중인 ‘독사조신(Doxazosin)’ 같은 약물이 이 신호를 차단하는 데 효과가 있다는 결과도 나왔습니다.
암 치료에 있어 ‘신경계 차단’이라는 전혀 새로운 전선이 구축된 셈입니다. [21, 23]
통증 조절의 혁명, 구강암과 마약성 진통제
구강암 환자들을 괴롭히는 가장 큰 고통 중 하나는 상상도 못 할 정도의 통증입니다.
게다가 마약성 진통제인 모르핀조차 금방 내성이 생겨 효과가 없어지곤 하죠.
2026년 2월 Science Signaling은 이 통증과 내성의 원인이 하나의 신호전달 경로에서 시작된다는 사실을 폭로했습니다. [24, 25, 26]
EGFR: 암의 성장 엔진에서 통증의 주범으로
뉴욕 대학교(NYU) 치과대학 이예(Yi Ye) 교수팀은 구강암 세포가 내뿜는 물질이 주변 감각 신경의 ‘상피세포 성장인자 수용체(EGFR)’를 자극한다는 것을 발견했습니다.
원래 EGFR은 세포 분열 신호를 전달하는 녀석인데, 신경세포에서는 통증 신호를 증폭하는 장치로 돌변합니다. [25, 26, 27]
자극받은 EGFR은 다시 ‘NMDA 수용체’라는 또 다른 통증 통로를 과활성화시킵니다.
NMDA 수용체는 우리 뇌와 척수에서 통증을 기억하고 강화하는 역할을 하는데, 이 녀석이 폭주하면 모르핀이 들어와도 그 효과를 비웃듯 강력한 통증 신호를 뇌로 쏴버립니다.
이것이 구강암 환자들이 진통제 내성을 그토록 빨리 겪는 이유였습니다. [25, 28]
연구팀은 이미 다른 암 치료에 쓰이고 있는 EGFR 억제제를 사용하면 통증이 드라마틱하게 줄어들 뿐만 아니라, 모르핀의 약효까지 되살아난다는 것을 쥐 실험을 통해 증명했습니다.
암 치료제가 진통제 내성을 해결하는 열쇠가 된 것이죠. [25, 28]
알기 쉬운 개념: EGFR
EGFR(Epidermal Growth Factor Receptor, 상피세포 성장인자 수용체)은 전형적인 원암유전자(Proto-oncogene)이며, 변이가 생겨 활성화되면 암을 일으키는 핵심적인 암유전자(Oncogene)로 돌변합니다.
역할: 정상적인 상태에서 EGFR은 세포막에 위치하며, 외부의 성장 신호(EGF 등)를 받아 세포에게 “분열하고 성장하라“는 명령을 전달하는 안테나 역할을 합니다.
EGFR에 변이가 생긴다면?
정상적인 EGFR은 신호 물질(리간드)이 결합할 때만 작동하지만, 변이가 생기면 신호가 없어도 스스로 계속 켜져 있는 상태(Constitutive activation)가 됩니다.
미토콘드리아의 지질 관리: Ayr1의 발견
세포의 발전소 미토콘드리아가 에너지만 만드는 줄 아셨다면 오산입니다.
최근 연구에 따르면 미토콘드리아는 세포 내의 지질(기름) 저장고를 직접 관리하고 있었습니다.
2026년 2월 Nature Cell Biology에 실린 독일 본 대학교 토마스 베커(Thomas Becker) 교수팀의 연구는 이 정교한 관리 시스템의 핵심 요소를 찾아냈습니다. [29, 30, 31]
세포 안에는 에너지를 저장하는 ‘지질 방울(Lipid Droplet)’이 떠다닙니다.
미토콘드리아는 이 지질 방울과 물리적으로 접촉하여 기름을 가져다 쓰는데, 이때 ‘Ayr1’이라는 효소가 접착제 역할을 합니다. [29, 30, 32]
보통 미토콘드리아 겉면에는 단백질을 안으로 집어넣는 통로(MIM 복합체)가 있는데, Ayr1은 특이하게도 이 통로에 딱 걸쳐진 채로 미토콘드리아 밖을 향해 팔을 뻗습니다.
그리고 지나가는 지질 방울을 낚아채 미토콘드리아 표면에 고정하죠. [30, 31, 32]
놀라운 것은 이 Ayr1이 미토콘드리아에 많이 붙어 있을수록 세포 내 전체 지질 방울의 개수가 늘어난다는 것입니다.
미토콘드리아가 자신의 에너지 수요에 맞춰 기름 창고의 규모를 스스로 결정하고 있다는 뜻이죠.
이 신호 체계에 문제가 생기면 비만이나 당뇨 같은 대사 질환으로 이어질 수 있습니다. [30, 31]
미토콘드리아를 물려받는 ‘금수저’와 ‘흙수저’
백신을 맞으면 우리 몸은 병균을 기억하는 ‘기억 T세포’를 만듭니다.
2026년 2월 Nature Cell Biology에서 막스 델브뤼크 센터(MDC) 연구팀은 T세포가 분열할 때 자가포식 시스템을 이용해 건강하고 쌩쌩한 미토콘드리아를 한쪽 딸 세포에만 몰아준다는 것을 발견했습니다. [33]
깨끗한 미토콘드리아를 물려받은 ‘금수저’ 세포는 오래 살아남아 우리 몸을 지키는 ‘기억 T세포’가 되고, 낡은 미토콘드리아를 받은 세포는 단기간에 적과 싸우고 장렬히 전사하는 ‘작동 세포’가 됩니다.
이 자가포식 경로를 조절하면 노인들의 백신 효과를 높일 수 있는 획기적인 길이 열릴지도 모릅니다. [33]
[개념쏙쏙] 알기 쉬운 세포 신호 개념
| 용어 | 쉬운 설명 | 관련 연구 결과 |
|---|---|---|
| JAK-STAT | 세포 밖의 신호를 핵까지 전달하는 초고속 통로 | CAR-T 세포 치료제 설계의 핵심 [36, 37] |
| cGAS-STING | 세포질에 있는 ‘수상한 DNA’를 감지하는 바이러스 알람 | 유전자 구조 붕괴 시 자가면역 반응 유도 [19] |
| mTOR | 세포의 성장을 결정하는 총사령관 | 암 대사 및 노화 억제 약물의 주요 타겟 [38, 39] |
| NF-κB | 염증과 생존 신호를 켜는 마스터 스위치 | 암 관련 섬유아세포(CAF) 조절에 관여 [40, 41] |
| Anoikis (아노이키스) | 집(세포 기질)을 떠난 세포가 외로워서 선택하는 자살 | 암세포가 전이되기 위해 극복해야 하는 단계 [42] |
| Exosome (엑소좀) | 세포들이 신호 물질을 담아 보내는 ‘택배 상자’ | 뇌 감염 진단 및 폐-눈 간 신호전달 매개 [43, 44] |
참고자료
- Cell signaling – Wikipedia, https://en.wikipedia.org/wiki/Cell_signaling
- Cell Signaling | Home Page – ProBiologists, https://www.probiologists.com/journal/Cell-Signaling
- Nature Cell Biology – Phys.org, https://phys.org/journals/nature-cell-biology/
- Weill Institute for Cell and Molecular Biology – Ithaca, New York, https://wicmb.cornell.edu/
- Vitamins: a tool to exploit against cancer – Lausanne – Unil, https://www.unil.ch/news/en/1770299899860
- Scientists Uncover Hidden Weakness in Cancer Cells Tied to Vitamin B7 – SciTechDaily, https://scitechdaily.com/scientists-uncover-hidden-weakness-in-cancer-cells-tied-to-vitamin-b7/
- Vitamins: A tool to exploit against cancer – EurekAlert!, https://www.eurekalert.org/news-releases/1116996
- Vitamins: A Powerful Ally in the Fight Against Cancer – Bioengineer.org, https://bioengineer.org/vitamins-a-powerful-ally-in-the-fight-against-cancer/
- Functional nutrient-genetic profiling reveals biotin and FBXW7 are essential to bypass glutamine addiction – ResearchGate, https://www.researchgate.net/publication/401216427_Functional_nutrient-genetic_profiling_reveals_biotin_and_FBXW7_are_essential_to_bypass_glutamine_addiction
- A hidden cellular process may drive aging and disease – ScienceDaily, https://www.sciencedaily.com/releases/2026/02/260203030526.htm
- Aging researchers find new puzzle piece in the game of longevity – EurekAlert!, https://www.eurekalert.org/news-releases/1114878
- (PDF) ER-phagy drives age-onset remodeling of endoplasmic reticulum structure-function and lifespan – ResearchGate, https://www.researchgate.net/publication/382986327_ER-phagy_drives_age-onset_remodeling_of_endoplasmic_reticulum_structure-function_and_lifespan
- ER remodelling is a feature of ageing and depends on ER-phagy – ResearchGate, https://www.researchgate.net/publication/400361917_ER_remodelling_is_a_feature_of_ageing_and_depends_on_ER-phagy
- Aging researchers find new puzzle piece in the game of longevity …, https://medschool.vanderbilt.edu/basic-sciences/2026/02/02/aging-researchers-find-new-puzzle-piece-in-the-game-of-longevity/
- Aging Cells Rewire their Protein Factories – The Scientist, https://www.the-scientist.com/aging-cells-rewire-their-protein-factories-74115
- Study on Worms Reveals New Adaptation to Cellular Aging – Boring Report, https://www.boringreport.org/app/article/6999469a12781b96524ea901
- New technology reveals hidden DNA scaffolding built before life …, https://www.eurekalert.org/news-releases/1117395
- New Tech Unveils Pre-Life DNA Scaffolding | Mirage News, https://www.miragenews.com/new-tech-unveils-pre-life-dna-scaffolding-1625389/
- Pico-C Reveals Pre-Life DNA Scaffolding | MRC LMS UK, https://www.academicjobs.com/research-publication-news/pico-c-reveals-pre-life-dna-scaffolding-or-mrc-lms-uk-research-6264
- Imaging Technique Reveals DNA’s Hidden Shape in the Earliest of Embryos, https://www.discovermagazine.com/imaging-technique-reveals-dna-s-hidden-shape-in-the-earliest-of-embryos-48747
- Scientists find nerves actively fuel pancreatic cancer | ScienceDaily, https://www.sciencedaily.com/releases/2026/02/260211204208.htm
- (PDF) Sympathetic nerve–fibroblast crosstalk drives nerve injury, fibroblast activation, and matrix remodeling in pancreatic cancer – ResearchGate, https://www.researchgate.net/publication/400963882_Sympathetic_nerve-fibroblast_crosstalk_drives_nerve_injury_fibroblast_activation_and_matrix_remodeling_in_pancreatic_cancer
- Let’s get on pancreatic cancer’s nerves – EurekAlert!, https://www.eurekalert.org/news-releases/1115636
- NYSDA News February 2026 Vol 39 No 1 – Issuu, https://issuu.com/brownst303/docs/nysda_news_february_2026_vol_39_no_1
- Shared Process Underlies Oral Cancer Pain and Opioid Tolerance, https://www.nyu.edu/about/news-publications/news/2026/january/oral-cancer-pain.html
- Shared Process Underlies Oral Cancer Pain and Opioid Tolerance | Dentistry33, https://www.dentistry33.com/news/editorials/5109/shared-process-underlies-oral-cancer-pain-and-opioid-tolerance.html
- Phenotypic drug screen uncovers the metabolic GCH1/BH4 pathway as key regulator of EGFR/KRAS-mediated neuropathic pain and lung cancer. – R Discovery, https://discovery.researcher.life/article/phenotypic-drug-screen-uncovers-the-metabolic-gch1-bh4-pathway-as-key-regulator-of-egfr-kras-mediated-neuropathic-pain-and-lung-cancer/370f0bb23a953b0fae159aaecdaefdce
- NYUHSL Faculty Bibliography, https://library.med.nyu.edu/api/publications?person=yy22
- Nature Cell Biology: Impact Factor, Ranking, H-Index, ISSN …, https://researcher.life/journal/nature-cell-biology/6773
- Mitochondria influence lipid storage in cells – CIBSS, https://www.cibss.uni-freiburg.de/news/mitochondria-influence-lipid-storage-in-cells-2
- Mitochondria Unveiled as the Cell’s Lipid Regulators – AZoLifeSciences, https://www.azolifesciences.com/news/20260227/Mitochondria-Unveiled-as-the-Celle28099s-Lipid-Regulators.aspx
- Vitasta Tiku’s research works | University of Bonn and other places – ResearchGate, https://www.researchgate.net/scientific-contributions/Vitasta-Tiku-2262558504
- What determines the fate of a T cell? – Max Delbrück Center, https://www.mdc-berlin.de/news/press/what-determines-fate-t-cell
- Bidirectional signals generated by Siglec-7 and its crucial ligand tri-sialylated T to escape of cancer cells from immune surveillance – ResearchGate, https://www.researchgate.net/publication/384848684_Bidirectional_signals_generated_by_Siglec-7_and_its_crucial_ligand_tri-sialylated_T_to_escape_of_cancer_cells_from_immune_surveillance
- Bufalin-Mediated Regulation of Cell Signaling Pathways in Different Cancers: Spotlight on JAK/STAT, Wnt/β-Catenin, mTOR, TRAIL/TRAIL-R, and Non-Coding RNAs – MDPI, https://www.mdpi.com/1420-3049/28/5/2231
- Abstract A013: Programmable JAK/STAT signaling drives CAR T cells to enhanced functional states | Cancer Immunology Research – AACR Journals, https://aacrjournals.org/cancerimmunolres/article/14/2_Supplement/A013/774271/Abstract-A013-Programmable-JAK-STAT-signaling
- Abstract A013: Programmable JAK/STAT signaling drives CAR T cells to enhanced functional states | Cancer Immunology Research – AACR Journals, https://aacrjournals.org/cancerimmunolres/article/14/2_Supplement/A013/774271
- Special Issue : Latest Review Papers in Molecular Biology 2026 – MDPI, https://www.mdpi.com/journal/cimb/special_issues/6VOYE10R60
- 4-Methoxydalbergione Induces Dual Activation of Apoptosis and Autophagy-Dependent Cell Death via ROS–MAPK Signaling in Human Neuroblastoma Cells – MDPI, https://www.mdpi.com/2073-4409/15/5/431
- Cells, Volume 15, Issue 3 (February-1 2026) – 100 articles – MDPI, https://www.mdpi.com/2073-4409/15/3
- BPS2026 – Signaling protein nucleation and condensation in the T-cell signaling pathway | Request PDF – ResearchGate, https://www.researchgate.net/publication/400953566_BPS2026_-_Signaling_protein_nucleation_and_condensation_in_the_T-cell_signaling_pathway
- TGFBR3 supports anoikis through suppressing ATF4 signaling | Journal of Cell Science, https://journals.biologists.com/jcs/article-abstract/135/17/jcs258396/276460/TGFBR3-supports-anoikis-through-suppressing-ATF4
- Exosomes in cerebrospinal fluid as biomarkers of bacterial infections of the central nervous system: a pilot study – Frontiers, https://www.frontiersin.org/journals/cellular-and-infection-microbiology/articles/10.3389/fcimb.2026.1760073/full
- Cells, Volume 15, Issue 4 (February-2 2026) – 75 articles – MDPI, https://www.mdpi.com/2073-4409/15/4
- Explore the Latest in Quantitative Cell Biology with MBoC – ASCB, https://www.ascb.org/science-news/explore-the-latest-in-quantitative-cell-biology-with-mboc/
- How the body really ages: 7 million cells mapped across 21 organs – ScienceDaily, https://www.sciencedaily.com/releases/2026/02/260228082717.htm
- New Microscopy Technique Lets Scientists See Cells in Unprecedented Detail and Color, https://www.biophysics.org/blog/new-microscopy-technique-lets-scientists-see-cells-in-unprecedented-detail-and-color
- Single cell and spatial transcriptomics highlight the interaction of club-like cells with immunosuppressive myeloid cells in prostate cancer – Queen’s University Belfast, https://pureadmin.qub.ac.uk/ws/portalfiles/portal/619185302/Kiviaho_et_al.pdf
- Chlorpromazine activates cGAS-STING signaling and reprograms the immune response in glioblastoma – Frontiers, https://www.frontiersin.org/journals/immunology/articles/10.3389/fimmu.2026.1743232/full
- Cell 2026 – Oxford Global, https://oxfordglobal.com/nextgen-biomed/events/cell
- Ten Cell Biology Conferences to Attend in 2026 – Hello Bio, https://hellobio.com/blog/ten-cell-biology-conferences-to-attend-in-2026.html
- American Journal of Physiology-Cell Physiology, https://journals.physiology.org/journal/ajpcell
- Cell Journals: Impact Factors & Key Publications 2024 – The Gambia College, https://www.gambiacollege.edu.gm/blog/cell-journals-impact-factors-and-key-publications-2024-1767646797
- The power of Science-based marketing., https://advertising.science.org/wp-content/uploads/2026/02/2026_Science_MediaKit_Final.pdf