우리는 흔히 우리 몸을 하나의 거대한 기계에 비유하곤 하지만, 사실 우리 몸은 그보다 훨씬 복잡하고 정교한 ‘초연결 스마트시티’에 가깝습니다.
수십 조 개의 세포들이 매 순간 수조 비트의 정보를 주고받으며 우리가 숨 쉬고, 걷고, 생각하고, 심지어 실수로부터 배우게 만듭니다.
이 통신 시스템을 우리는 ‘세포 신호전달(Cell Signaling)’이라고 부릅니다. 만약 이 통신망에 아주 작은 노이즈가 생기거나 암호 체계가 바뀐다면 어떻게 될까요?
선천 면역의 새로운 암호 체계: ANKIB1과 리신-11 유비퀴틴화
우리의 면역 체계는 외부 침입자를 감지하는 즉시 복잡한 신호탄을 쏘아 올립니다.
그중에서도cGAS-STING 경로는 바이러스의 DNA를 감지해 인터페론이라는 강력한 항바이러스 물질을 만들어내는 핵심 통로입니다.
그런데 최근 Nature Cell Biology에 발표된 연구에 따르면, 이 통로가 제대로 작동하기 위해서는 우리가 그동안 과소평가했던 ‘리신-11(K11)’이라는 특수한 유비퀴틴 암호가 반드시 필요하다는 사실이 밝혀졌습니다.[1, 2]
ANKIB1, 면역 신호의 새로운 설계자
단백질에 유비퀴틴이라는 작은 태그를 붙이는 ‘유비퀴틴화’는 보통 단백질의 운명을 결정합니다.
리신-48(K48) 태그가 붙으면 쓰레기통으로 가고, 리신-63(K63) 태그가 붙으면 신호를 활성화하죠.
하지만 Betrancourt 박사팀은 ANKIB1이라는 E3 리가아제가 생성하는 K11 연결 유비퀴틴 사슬이 인터페론 유도의 ‘마스터 키’임을 입증했습니다.[2]
ANKIB1은 TLR3와 cGAS-STING 신호 복합체에 이 특수한 K11 사슬을 붙여서, 옵티뉴린(Optineurin)이라는 단백질을 불러모으는 물리적인 발판을 만듭니다.[3, 4]
이 발판이 있어야만 면역의 핵심 장군인 TBK1과 IRF3가 활성화되어 항바이러스 유전자를 깨울 수 있습니다.
면역 결핍과 바이러스 저항성의 상관관계
이 신호 체계의 중요성은 동물을 통한 실험에서 더욱 명확해졌습니다.
연구팀이 ANKIB1 단백질을 만들지 못하게 유전자를 조작한 마우스는 단순 포진 바이러스(HSV-1) 감염에 매우 취약한 모습을 보였습니다.[3, 4]
이는 우리 몸이 바이러스와 싸울 때 단순히 신호를 보내는 것뿐만 아니라, 그 신호를 얼마나 정교한 ‘화학적 구조물’ 위에 쌓아 올리느냐가 생존을 결정한다는 것을 의미합니다.
이 발견은 향후 자가면역 질환이나 바이러스 감염병 치료에서 ANKIB1을 조절하는 새로운 전략을 세우는 데 결정적인 단서가 될 것으로 보입니다.[2]
[개념 쏙쏙] 유비퀴틴화
단백질의 유비퀴틴화(Ubiquitination)는 단순히 단백질을 쓰레기통으로 보내는 표식이 아니라, 단백질의 ‘운명’을 결정하는 정교한 세포 내 우편 시스템과 같습니다.
유비퀴틴화는 세 가지 효소의 순차적인 작용으로 일어나는 매우 체계적인 화학 결합 과정입니다.
- E1 (활성화 효소, Activating Enzyme): ATP를 사용하여 유비퀴틴 단백질을 활성화합니다.
- E2 (결합 효소, Conjugating Enzyme): 활성화된 유비퀴틴을 전달받아 E3 효소로 옮깁니다.
- E3 (연결 효소, Ligase): 가장 중요한 단계로, 특정 타겟 단백질을 인식하여 유비퀴틴을 부착합니다. 우리 몸에는 수백 종류의 E3가 있어 각기 다른 단백질을 선별합니다.
유비퀴틴화의 운명은 ‘개수‘와 ‘연결 방식‘에 의해 결정됩니다.
K63 연결 (Lysine 63): 분해되지 않습니다. 대신 염증 신호 전달(NF-$kappa$B 활성), DNA 손상 복구 등을 수행합니다.
단일 유비퀴틴화 (Monoubiquitination): 단백질에 유비퀴틴이 딱 하나 붙는 경우입니다. 주로 분해가 아니라 세포 내 신호 전달, DNA 복구, 내포 작용(Endocytosis) 등을 조절하는 스위치 역할을 합니다.
다중 유비퀴틴화 (Polyubiquitination): 유비퀴틴 여러 개가 사슬처럼 엮이는 경우입니다. 여기서 ‘어느 지점‘에서 연결되느냐가 핵심입니다.
K48 연결 (Lysine 48): 이것이 질문하신 ‘분해‘의 신호입니다. 프로테아좀(Proteasome)으로 보내져 파괴됩니다.
[개념 쏙쏙] 유비퀴틴 체인에서 리신의 역할
연결 부위에 따른 기능의 차이
유비퀴틴은 그 자체로 단백질입니다. 단백질은 아미노산 체인으로 구성되는데, 유비퀴틴 안에는 총 7개의 리신(K6, K11, K27, K29, K33, K48, K63)이 존재합니다.
- 리신 48 (K48): 유비퀴틴 단백질의 48번째 아미노산이 리신인 지점입니다.
- 리신 63 (K63): 유비퀴틴 단백질의 63번째 아미노산이 리신인 지점입니다.
유비퀴틴 사슬(Polyubiquitin chain)이 형성될 때, 첫 번째 유비퀴틴의 특정 리신 잔기에 두 번째 유비퀴틴의 말단(C-terminus)이 결합합니다. 이때 ‘몇 번 리신’을 통해 연결 되느냐에 따라 사슬의 입체 구조가 결정됩니다.
연결 부위에 따른 기능의 차이
| 구분 | 주요 기능 | 메커니즘 |
| K48 연결 | 단백질 분해 | 사슬이 닫힌(Closed) 구조를 형성하여 프로테아좀(26S Proteasome)이 인식하게 함. |
| K63 연결 | 신호 전달 / DNA 수선 | 사슬이 열린(Open/Linear) 구조를 형성하여 분해보다는 단백질 간의 상호작용을 매개함. |
[개념 쏙쏙] cGAS-STING
cGAS-STING 경로는 세포가 외부 침입자(바이러스, 세균)나 내부의 손상된 DNA를 감지하여 선천 면역 반응을 일으키는 핵심적인 감시 체계입니다.
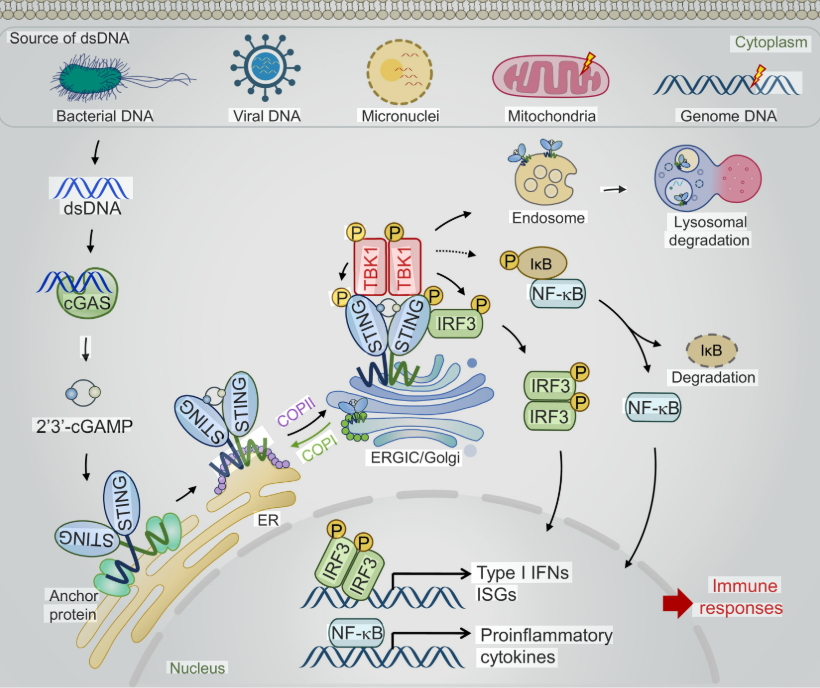
1. dsDNA의 유입 및 감지 (Source of dsDNA)
세포질은 본래 DNA가 없어야 하는 공간입니다. 하지만 다음과 같은 상황에서 이중 가닥 DNA(dsDNA)가 나타날 수 있습니다:
- 외인성: 세균(Bacterial)이나 바이러스(Viral)의 감염.
- 내인성: 손상된 핵에서 나온 미세핵(Micronuclei), 미토콘드리아(Mitochondria) 손상으로 유출된 DNA, 혹은 게놈 DNA의 비정상적 유출.
이때 세포질에 존재하는 효소인 cGAS가 이 dsDNA를 감지하여 결합합니다.
2. 제2메신저 cGAMP 생성
cGAS가 dsDNA와 결합하면 활성화되어, 세포 내의 ATP와 GTP를 사용하여 2’3′-cGAMP라는 제2메신저를 합성합니다.
3. STING의 활성화와 이동
- ER(소포체) 막에 위치하던 STING 단백질이 cGAMP와 결합합니다.
- 활성화된 STING은 ER에서 나와 ERGIC(소포체-골지 중간 구획)를 거쳐 골지체(Golgi)로 이동합니다. 이 과정에서 COPII 소낭이 관여합니다.
4. 신호 전달 및 인산화 (Signaling Cascade)
골지체 근처에서 STING은 TBK1 인산화 효소를 모집합니다.
- IRF3 경로: TBK1이 IRF3를 인산화시키면, 인산화된 IRF3는 이합체(Dimer)를 형성하여 핵 안으로 들어갑니다.
- NF-κB 경로: 동시에 IκB의 인산화 및 분해를 유도하여 NF-κB 전사 인자를 자유롭게 만들어 핵으로 보냅니다.
5. 면역 반응 유도 (Immune Responses)
핵으로 들어간 전사 인자들은 특정 유전자들의 발현을 촉진합니다:
- Type I IFNs (제1형 인터페론): 바이러스 증식을 억제합니다.
- ISGs (인터페론 자극 유전자): 항바이러스 상태를 유도합니다.
- Proinflammatory cytokines: 염증 반응을 일으켜 면역 세포들을 불러 모읍니다.
6. 경로의 종료
신호 전달을 마친 STING은 엔도좀(Endosome)을 거쳐 리소좀(Lysosome)으로 이동하여 분해됨으로써 과도한 면역 반응이 일어나지 않도록 조절됩니다.
뇌의 ‘실수 학습’을 가능하게 하는 숨겨진 회로
우리는 걷다가 발을 헛디디거나 악기를 연주하다 음을 틀렸을 때, 다음번에는 똑같은 실수를 하지 않도록 몸을 교정합니다.
이 놀라운 학습 능력은 뇌 뒤쪽에 위치한 소뇌(Cerebellum) 덕분입니다.
등반 섬유의 역설과 탈억제 메커니즘
소뇌에는 ‘등반 섬유(Climbing fibers)‘라고 불리는 신경이 있는데, 이들은 운동이 계획대로 되지 않았을 때 강력한 에러 신호를 보냅니다.
이 신호는 소뇌의 출력 담당인 푸르키네 세포(Purkinje cells)에서 칼슘 분출을 일으켜 신경 연결을 재구성(Plasticity)하게 만듭니다.[5]
하지만 과학자들은 오랫동안 한 가지 역설에 빠져 있었습니다.
등반 섬유가 학습을 촉진하는 동시에, 학습을 방해하는 억제성 세포들도 함께 활성화시킨다는 점이었죠.
Duke 대학의 Court Hull 교수팀은 이 역설이 사실은 ‘브레이크를 끄는 브레이크’ 시스템을 통해 해결된다는 것을 알아냈습니다.[5]
실수를 학습으로 : 학습의 문을 여는 이중 잠금장치
연구팀은 초고해상도 전자현미경을 통해 등반 섬유가 특정 억제 세포인 ML12를 우선적으로 활성화한다는 것을 발견했습니다.[5]
놀랍게도 ML12 세포는 푸르키네 세포를 직접 억제하는 게 아니라, 다른 억제 세포인 ML11을 공격합니다.
평소에 ML11은 학습이 일어나지 않도록 푸르키네 세포를 꽉 누르고 있는데, 등반 섬유가 ML12를 시켜 ML11(브레이크)을 잠시 제거해주면, 그제야 푸르키네 세포가 강력한 칼슘 신호를 내뿜으며 학습을 시작하게 되는 것입니다.[5]
이러한 정교한 ‘탈억제(Disinhibition)‘ 과정은 우리가 큰 실수를 했을 때 뇌가 비로소 학습의 문을 활짝 여는 이유를 설명해줍니다.
| 뉴런 유형 | 주요 기능 및 역할 | 특징 |
|---|---|---|
| 등반 섬유 | 에러 신호(Error signal) 전달 | 학습의 트리거 역할 [5] |
| ML12 세포 | ML11 세포를 억제하여 브레이크 해제 | 이번 연구에서 밝혀진 핵심 매개체 [5] |
| ML11 세포 | 평상시 푸르키네 세포의 가소성 억제 | 학습을 방해하는 내부 브레이크 [5] |
| 푸르키네 세포 | 칼슘 신호를 통한 시냅스 재배선 | 소뇌의 최종 정보 처리 및 출력 [5] |
[개념 쏙쏙] 등반 섬유와 푸르키네 세포
푸르키네 세포 (Purkinje Cell): 소뇌 피질에서 가장 크고 복잡한 뉴런입니다. 매우 거대한 수지상 돌기(Dendrite)를 2차원 평면으로 펼치고 있으며, 소뇌 피질의 유일한 출력(Output) 경로입니다. 이 세포의 축삭은 소뇌 심부핵으로 억제성 신호(GABA)를 보냅니다.
등반 섬유 (Climbing Fiber): 뇌간의 하올리브핵(Inferior Olive)에서 시작됩니다. 하나의 등반 섬유는 하나의 푸르키네 세포를 마치 덩굴식물이 나무를 감고 올라가듯 촘촘하게 감싸며 수천 개의 시냅스를 형성합니다.
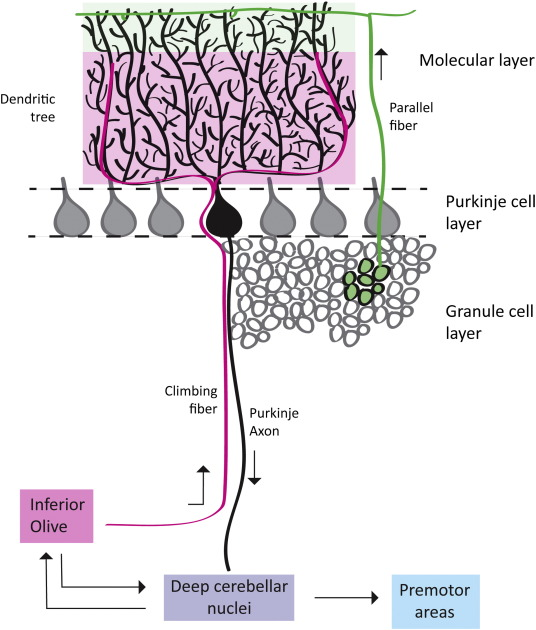
푸르키네 세포는 두 가지 형태의 전기적 활성(Spike)을 보입니다.
복합 반응 (Complex Spike): 등반 섬유가 자극될 때 발생합니다. 한 번의 자극으로 푸르키네 세포 전체에 강력한 탈분극이 일어나며, 큰 파동 뒤에 작은 파동들이 이어지는 독특한 파형을 보입니다. 초당 1회 정도로 매우 드물게 발생합니다.
단순 반응 (Simple Spike): 이끼 섬유(Mossy Fiber)로부터 오는 평행 섬유의 자극으로 발생하며, 초당 50~100회 정도로 빈번하게 일어납니다. 평상시의 운동 제어와 관련이 있습니다.
세포의 뼈대가 신호를 보낸다? 스펙트린과 역학적 신호전달
우리는 세포막이 단순히 세포를 감싸는 봉투라고 생각하기 쉽지만, 사실 그 안에는 ‘스펙트린(Spectrin)‘이라는 튼튼한 그물망 골격이 존재합니다.
2026년 3월 Journal of Cell Biology(JCB)에 실린 연구는 이 스펙트린 골격이 피부의 장벽을 형성하고 세포의 운명을 결정하는 중요한 신호 조절자임을 보여주었습니다.[6, 7]
피부 장벽의 설계자, αII-스펙트린
피부의 가장 바깥층인 표피가 외부 세균을 막는 튼튼한 장벽이 되기 위해서는 각질세포들이 아주 정교하게 줄을 맞추고 변신해야 합니다.
Soffer 등은 αII-스펙트린이 세포막에서 상피세포 성장인자 수용체(EGFR)와 TRPV3 이온 채널을 한데 묶어주는 ‘비계’ 역할을 한다는 사실을 밝혀냈습니다.[6]
스펙트린 골격이 이들을 딱 붙여놓아야만 피부 장벽 형성 효소인 TGM1이 활성화될 수 있습니다.
만약 스펙트린이 부족하면, 세포는 제 모양을 갖추지 못하고 피부 장벽이 무너져 각종 염증과 질환에 노출되게 됩니다.[6, 7]
물리적 힘을 화학적 신호로 바꾸는 기법
더욱 흥미로운 점은 이 과정이 ‘역학적 피드백’을 기반으로 한다는 것입니다.
EGFR 신호가 전달되면 세포 내부의 수축력이 강해지고, 이 물리적 힘이 다시 스펙트린 골격을 통해 신호를 강화하는 선순환 구조를 가집니다.[6, 7]
이는 세포가 단순히 주변의 화학 물질 농도만 체크하는 것이 아니라, 자신이 처한 물리적 압력과 위치를 ‘느끼고’ 이에 맞춰 신호전달 강도를 조절한다는 것을 시사합니다.[7]
이 연구는 조직 공학이나 재생 의학에서 세포의 형태와 골격을 조절하는 것이 얼마나 중요한지 다시 한번 일깨워줍니다.
[과학 쏙쏙] 역학적 신호전달 (Mechanotransduction)
세포가 외부의 물리적 자극(압력, 신장, 전단 응력 등)을 감지하여 이를 세포 내 화학적 신호로 바꾸는 과정을 말합니다.
의의: 암을 제외한 일반적인 조직 발달, 혈류 감지, 청각 형성 등에 필수적인 경로입니다.[8, 9]
핵심 인자: 세포막의 이온 채널, 세포 골격(액틴, 스펙트린), 접착 단백질(인테그린, 카데린).[6]
[과학 쏙쏙] 스펙트린
스펙트린은 세포막 바로 안쪽에서 골격을 형성하는 거대 섬유상 단백질입니다.
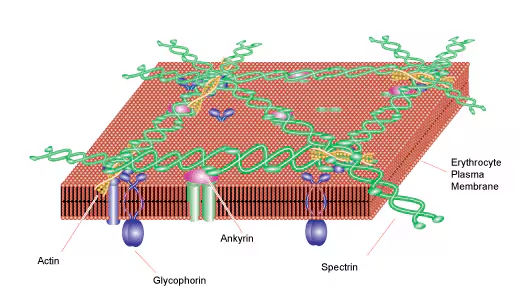
적혈구에서의 역할: 적혈구가 좁은 모세혈관을 통과할 때 파괴되지 않고 형태를 회복할 수 있는 유연성과 탄성을 제공합니다.
기본 구조: α-스펙트린과 β-스펙트린이라는 두 개의 사슬이 서로 꼬여 이합체(Heterodimer)를 형성하고, 이 이합체 두 개가 머리를 맞대어 사합체(Tetramer)를 이룹니다. 이 사합체가 스펙트린 골격의 기본 단위가 됩니다.
세포막 고정: 스펙트린은 스스로 막에 붙지 못합니다. 안키린(Ankyrin)이라는 매개 단백질을 통해 세포막의 이온 통로(Band 3 등)와 연결되거나, 엑틴(Actin) 필라멘트와 결합하여 견고한 네트워크를 형성합니다.
여성이 장 질환에 더 민감한 이유
과민성 대장 증후군(IBS)과 같은 질환은 남성보다 여성에게서 훨씬 더 흔하게 나타납니다.
2026년 3월 Nature지에 발표된 연구는 그 원인이 장내 세포들 사이의 ‘에스트로겐 민감형 대화’에 있다는 것을 세포 수준에서 규명했습니다.[10]
PYY와 세로토닌의 위험한 협동
연구진은 장 상피의 L 세포와 EC 세포라는 두 종류의 내분비 세포가 여성 호르몬인 에스트로겐의 지휘 아래 움직인다는 것을 확인했습니다.[10]
- 에스트로겐은 L 세포에 있는 미생물 대사체 수용체(Olfr78)의 발현을 높입니다.
- 이 수용체는 장내 미생물이 만드는 아세테이트(Acetate)를 감지하여 L 세포가 PYY라는 신호 물질을 더 많이 뿜어내게 합니다.
- 늘어난 PYY는 바로 옆에 있는 EC 세포를 자극해 엄청난 양의 세로토닌을 방출하게 만듭니다.
- 이 세로토닌이 장의 감각 신경을 과도하게 자극하여 통증과 민감도를 대폭 높이는 것입니다.[10]
이 발견은 여성의 장 민감도가 단순히 심리적인 요인이 아니라, 호르몬과 미생물 대사체가 얽힌 정교한 세포 신호전달의 결과임을 보여줍니다.
이는 성별에 따른 맞춤형 장 질환 치료제 개발의 새로운 문을 연 것으로 평가받고 있습니다.
치아와 신경을 되살리는 신호 스위치
손상된 조직을 되살리는 일은 하나의 세포 재생의 혁신으로 볼 수 있습니다. 2026년 3월, 치아와 신경 재생 분야에서 각각 혁신적인 신호 경로가 발견되었습니다.[11, 12]
SMAD7: 치아 재생의 반전 주인공
보통 SMAD7은 성장을 억제하는 단백질로 알려져 있었습니다.
하지만 치수 줄기세포(hDPSCs)에서는 이야기가 다릅니다. International Journal of Oral Science에 게재된 연구에 따르면, SMAD7은 핵 안에서 β-카테닌과 직접 손을 잡고 Wnt 신호를 강화하여 치아 조직의 재생을 돕는 ‘긍정적 리더’로 활약합니다.[11]
이 메커니즘을 잘 활용하면 힘든 신경치료 대신 치아 스스로의 생명력을 이용한 재생 치료가 가능해질 전망입니다.
신경 수복의 내비게이션, PPAR-γ/RhoA/ROCK
사고로 끊어진 말초 신경을 잇는 데 사용되는 도관(Conduit)이 어떻게 신경의 길잡이 역할을 하는지도 밝혀졌습니다.
최신 연구에 따르면, 특수 도관이 PPAR-γ/RhoA/ROCK 경로를 조절하여 신경 섬유인 축삭이 올바른 방향으로 뻗어 나가고, 이를 감싸는 마이엘린 수초가 두껍게 형성되도록 돕습니다.[12]
이는 마비 환자들의 기능 회복을 위한 스마트 보조 도구 개발에 핵심적인 데이터를 제공합니다.
| 재생 타겟 | 핵심 신호 경로 | 작용 기전 | 기대 효과 |
|---|---|---|---|
| 치아 (치수) | SMAD7 / Wnt / β-catenin | 줄기세포 분화 및 조직 수복 활성화 | 생물학적 치아 보존 치료 [11] |
| 말초 신경 | PPAR-γ / RhoA / ROCK | 축삭 재생 및 마이엘린 형성 촉진 | 신경 손상 환자의 운동 기능 회복 [12] |
| 망막 (MG 세포) | Notch signaling / Cell cycle | 휴면 세포의 재활성화를 통한 뉴런 생성 | 시력 상실 환자의 신경 재생 [13] |
[개념 쏙쏙] β-카테닌과 wnt signal pathway
세포 외부의 Wnt 단백질이 세포 표면의 수용체에 결합하여 세포 내부의 유전자 발현을 조절하는 복잡한 시스템입니다.
- Wnt 리간드: 세포 밖으로 분비되는 신호 전달 단백질 (인간에게는 19종 존재).
- 수용체 (Frizzled & LRP5/6): 세포막에서 Wnt 신호를 받아들이는 안테나 역할.
- β-카테닌 (핵심 인자): 평소에는 분해되다가, 신호가 오면 핵으로 들어가 유전자를 켭니다.
- 파괴 복합체 (Destruction Complex): β-카테닌을 붙잡아 분해시키는 청소부 그룹 (APC, Axin, GSK3β 등으로 구성).
Wnt 신호 전달은 크게 정상 경로(Canonical)와 비정상 경로(Non-canonical)로 나뉩니다. 여기서 β-카테닌은 ‘Canonical 경로’의 핵심 전사 활성 인자입니다.
유전자 발현 조절: 핵으로 들어온 β-카테닌은 TCF/LEF 전사 인자와 결합하여 c-Myc, Cyclin D1 등 세포 증식에 관여하는 표적 유전자의 발현을 촉진합니다.
식물의 생존 지혜: 가스 신호와 공생의 미학
식물도 우리만큼이나 복잡한 신호 체계를 가지고 있습니다. 2026년 3월, Plant Physiology 등 식물학 저널들은 식물이 흙을 뚫고 올라오거나 미생물과 친구가 될 때 사용하는 비밀 암호를 공개했습니다.
벼의 ‘토양 탈출 작전’과 에틸렌 신호
벼 씨앗이 깊은 흙 속에서 싹을 틔울 때, 이들은 에틸렌(Ethylene) 가스를 신호로 사용합니다.[14]
에틸렌 신호가 전달되면 OsEIL1과 OsEIL2라는 단백질이 활성화되어 세포 내의 활성산소(ROS)를 제거하는 효소들을 깨웁니다.
덕분에 벼의 초엽은 적절한 농도의 ROS를 유지하며 가늘고 길게 자라 흙을 더 쉽게 뚫고 나올 수 있게 됩니다.[14]
나무와 버섯의 우정, CLE 펩타이드
나무 뿌리가 토양 속 유익한 버섯(공생 균류)을 감지하고 받아들일 때는 CLE 펩타이드라는 작은 단백질 신호탄을 사용합니다.[15]
포플러 나무 연구에서 밝혀진 이 신호 경로는 나무가 척박한 땅에서도 영양분을 잘 흡수할 수 있도록 공생 관계를 조절하는 핵심 장치입니다.
이는 지속 가능한 산림 자원 관리와 친환경 농업을 위한 중요한 열쇠가 될 것입니다.
참고자료
- (9246) Phospho-IkappaB alpha (Ser32/36) (5A5) Mouse Monoclonal Antibody – CiteAb, https://www.citeab.com/antibodies/125948-9246-phospho-ikappab-alpha-ser32-36-5a5-mouse-mon
- (PDF) Lysine-11 ubiquitination drives type-I/III interferon induction by cGAS–STING and Toll-like receptors 3 and 4 – ResearchGate, https://www.researchgate.net/publication/401652008_Lysine-11_ubiquitination_drives_type-IIII_interferon_induction_by_cGAS-STING_and_Toll-like_receptors_3_and_4
- Bianca Buratti’s research works | University of Cologne and other places – ResearchGate, https://www.researchgate.net/scientific-contributions/Bianca-Buratti-2342399508
- Kerstin Becker’s research works | University of Cologne and other places – ResearchGate, https://www.researchgate.net/scientific-contributions/Kerstin-Becker-2342382579
- Hidden circuit helps the brain learn from mistakes | Duke University School of Medicine, https://medschool.duke.edu/news/hidden-circuit-helps-brain-learn-mistakes
- Bridging scales for cellular communities | Journal of Cell Biology …, https://rupress.org/jcb/article/225/4/e202602015/281568/Bridging-scales-for-cellular-communitiesSpectrin
- Bridging scales for cellular communities | Journal of Cell Biology …, https://rupress.org/jcb/article/225/4/e202602015/281568/Bridging-scales-for-cellular-communities
- Super-Resolution Imaging Reveals PIP2 Nanoscale Clusters in Immune Cells, https://www.biophysics.org/blog/super-resolution-imaging-reveals-pip2-nanoscale-clusters-in-immune-cells
- mTORC2 regulates auditory hair cell structure and function – ResearchGate, https://www.researchgate.net/publication/373221502_mTORC2_regulates_auditory_hair_cell_structure_and_function
- A Cellular Basis for Heightened Gut Sensitivity in Females – PMC – NIH, https://pmc.ncbi.nlm.nih.gov/articles/PMC12994136/
- New molecular switch that boosts tooth regeneration discovered – EurekAlert!, https://www.eurekalert.org/news-releases/1119183
- (PDF) The GDNF-Gel/HA-Mg conduit promotes the repair of peripheral nerve defects by regulating PPAR-γ/RhoA/ROCK signaling pathway – ResearchGate, https://www.researchgate.net/publication/377582561_The_GDNF-GelHA-Mg_conduit_promotes_the_repair_of_peripheral_nerve_defects_by_regulating_PPAR-gRhoAROCK_signaling_pathway
- Synergistic Inhibition of Notch Signaling and Forced Cell Cycle Re-entry Drive Müller Glia Reprogramming in Uninjured Mouse Retina | bioRxiv, https://www.biorxiv.org/content/10.64898/2026.03.09.710684v1
- OsEIL1 and OsEIL2, two master regulators of rice ethylene signaling, promote the expression of ROS scavenging genes to facilitate coleoptile elongation and seedling emergence from soil – ResearchGate, https://www.researchgate.net/publication/375845400_OsEIL1_and_OsEIL2_two_master_regulators_of_rice_ethylene_signaling_promote_the_expression_of_ROS_scavenging_genes_to_facilitate_coleoptile_elongation_and_seedling_emergence_from_soil
- Poplar CLE peptides promoting ectomycorrhizal symbiosis identified through genome-wide analysis of responsive small secreted peptides | Plant Physiology | Oxford Academic, https://academic.oup.com/plphys/article/200/3/kiag071/8495628